Hvad er valensbindingsbilledet af C2H2?
Valensbindingsbilledet af C2H2 kan repræsenteres som følger:
```
H-C=C-H
```
I denne repræsentation er sigma-bindingen mellem de to carbonatomer repræsenteret af den fuldt optrukne linje, og de to pi-bindinger mellem carbonatomerne og hydrogenatomerne er repræsenteret med de stiplede linjer.
 Varme artikler
Varme artikler
-
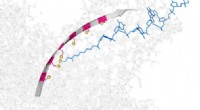 Molekylær tragt lille nok til at flytte enkelt DNA-strengeKredit:University of Oxford Forskere fra University of Oxford har konstrueret en molekylær beholder, i stand til at flytte enkeltstrenge af DNA gennem et protein nanorør. Den lille tragt fungere
Molekylær tragt lille nok til at flytte enkelt DNA-strengeKredit:University of Oxford Forskere fra University of Oxford har konstrueret en molekylær beholder, i stand til at flytte enkeltstrenge af DNA gennem et protein nanorør. Den lille tragt fungere -
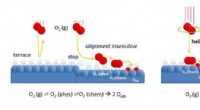 Vi forstår endelig, hvordan ilt reagerer på platinFigur til venstre:Iltmolekyler nærmer sig katalysatoroverfladen med lav hastighed. Trinene på overfladen spreder molekylerne til en svagt bundet fysisksorberet tilstand. Derfra, molekylerne kan nemt f
Vi forstår endelig, hvordan ilt reagerer på platinFigur til venstre:Iltmolekyler nærmer sig katalysatoroverfladen med lav hastighed. Trinene på overfladen spreder molekylerne til en svagt bundet fysisksorberet tilstand. Derfra, molekylerne kan nemt f -
 De stiveste porøse letvægtsmaterialer nogensindePladegitter er det valgmæssige design til fremtidige lette porøse materialer. Kredit:ETH Zürich / Marc Day Forskere ved ETH har udviklet og fremstillet en familie af arkitekturer, der maksimerer s
De stiveste porøse letvægtsmaterialer nogensindePladegitter er det valgmæssige design til fremtidige lette porøse materialer. Kredit:ETH Zürich / Marc Day Forskere ved ETH har udviklet og fremstillet en familie af arkitekturer, der maksimerer s -
 Strækbare og klemme bløde sensorer et skridt nærmere takket være den nye bindingsmetodeEn sensor holdt mellem to fingre. Kredit:Michael Kasimatis Bioingeniører fra Imperial College London har fundet en måde at skabe elastiske og squeezy bløde sensorenheder ved at binde gummi til ele
Strækbare og klemme bløde sensorer et skridt nærmere takket være den nye bindingsmetodeEn sensor holdt mellem to fingre. Kredit:Michael Kasimatis Bioingeniører fra Imperial College London har fundet en måde at skabe elastiske og squeezy bløde sensorenheder ved at binde gummi til ele
- Den tropiske storm Debby forventes at sende oversvømmelser mod sydøst. Her er, hvor meget regn der…
- Perception betyder noget:Hvordan frygt for kriminalitet påvirker præsidentens godkendelse
- Forskere sætter et nyt twist på grafit
- Brug af Google Street View til at estimere rejsemønstre i byer
- Hvordan nonprofitorganisationer kan booste donationer ved hjælp af marketingmixet
- Undersøgelse undersøger de bedste ledelsesmåder for iværksættere


