hvad er molariteten af H30?
For at beregne molariteten af hydroniumioner skal du kende koncentrationen af hydroniumioner i mol pr. liter. Denne information opnås normalt ved at måle opløsningens pH. En opløsnings pH er et mål for dens surhed eller basicitet, og den er omvendt proportional med hydrogenionkoncentrationen. Jo lavere pH-værdi, jo højere hydrogenionkoncentration og omvendt.
Når du kender opløsningens pH, kan du bruge følgende formel til at beregne molariteten af hydroniumioner:
```
[H3O+] =10^(-pH)
```
For eksempel, hvis pH af en opløsning er 3, kan molariteten af hydroniumioner beregnes som følger:
```
[H3O+] =10^(-3) =0,001 M
```
Derfor er molariteten af hydroniumioner i en opløsning med en pH på 3 0,001 M.
Sidste artikelHvilke af disse er bronstead-baser - HCl NH3 NaOH?
Næste artikelObservation under reaktionen af calciumcarbonat og saltsyre?
 Varme artikler
Varme artikler
-
 Sensoren kan registrere fordærvet mælk, før den åbnesDen eksperimentelle opsætning til påvisning af de flygtige forbindelser i mælk, med de lyserøde nanopartikler set over væsken. Kredit:WSU Udløbsdatoer på mælk kan i sidste ende blive fortid med ny
Sensoren kan registrere fordærvet mælk, før den åbnesDen eksperimentelle opsætning til påvisning af de flygtige forbindelser i mælk, med de lyserøde nanopartikler set over væsken. Kredit:WSU Udløbsdatoer på mælk kan i sidste ende blive fortid med ny -
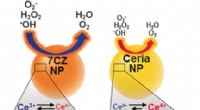 Ceria-zirconia nanopartikler som forbedrede multi-antioxidanter er effektive til behandling af sepsi…Kredit:Wiley Under sepsis, celler er oversvømmet med reaktive iltarter, der genereres i et afvigende respons fra immunsystemet på en lokal infektion. Hvis denne fatale inflammatoriske vej kunne fo
Ceria-zirconia nanopartikler som forbedrede multi-antioxidanter er effektive til behandling af sepsi…Kredit:Wiley Under sepsis, celler er oversvømmet med reaktive iltarter, der genereres i et afvigende respons fra immunsystemet på en lokal infektion. Hvis denne fatale inflammatoriske vej kunne fo -
 Svejsning med stamceller til næste generations kirurgiske limKredit:CC0 Public Domain Forskere ved University of Bristol har opfundet en ny teknologi, der kan føre til udviklingen af en ny generation af smarte kirurgiske lim og forbindinger til kroniske s
Svejsning med stamceller til næste generations kirurgiske limKredit:CC0 Public Domain Forskere ved University of Bristol har opfundet en ny teknologi, der kan føre til udviklingen af en ny generation af smarte kirurgiske lim og forbindinger til kroniske s -
 Hårfarve er giftigt – kan naturlige alternativer fås til at virke?Henna hårfarve er naturligt, men begrænset. Kredit:fotolotos/Shutterstock Ved du virkelig, hvad du sætter på dit hår? Mange hårfarver, du kan købe i butikkerne eller frisøren, indeholder giftige k
Hårfarve er giftigt – kan naturlige alternativer fås til at virke?Henna hårfarve er naturligt, men begrænset. Kredit:fotolotos/Shutterstock Ved du virkelig, hvad du sætter på dit hår? Mange hårfarver, du kan købe i butikkerne eller frisøren, indeholder giftige k
- Kan morfologien af fossile blade fortælle os, hvordan tidligt blomstrende planter voksede?
- Sådan fjerner du en kvadratrød i en ligning
- Skogbrande på østkysten af Australien ude af kontrol
- Hvordan aerosoler dannes
- Bakterielle nanoporer åbner fremtiden for datalagring
- Maskinlæring afdækker signaturen for langsomt glidende jordskælvs oprindelse i seismiske data


