Hvad er en måde at holde styr på valenselektroner i en ionforbindelse?
Na Cl
. .
. .
Natriumatomet har en valenselektron, som er repræsenteret ved prikken på venstre side af natriumsymbolet. Kloratomet har syv valenselektroner, som er repræsenteret af de syv prikker på højre side af klorsymbolet.
Det samlede antal valenselektroner i en ionisk forbindelse er lig med summen af valenselektronerne for alle atomerne i forbindelsen. For natriumchlorid er det samlede antal valenselektroner 8 (1 valenselektron fra natrium + 7 valenselektroner fra klor).
Lewis-punktstrukturen kan bruges til at bestemme ladningen på en ion. Ladningen på en ion bestemmes af forskellen mellem antallet af valenselektroner og antallet af protoner i ionen. For eksempel, i tilfælde af natriumchlorid, har natriumionen en ladning på +1, fordi den har en valenselektron og 11 protoner. Chloridionen har en ladning på -1, fordi den har syv valenselektroner og 17 protoner.
Sidste artikelEr der nikkel i tidevandsopvaskemiddel?
Næste artikelNår natrium opløses i vand, hvorfor begynder ilden at brænde?
 Varme artikler
Varme artikler
-
 Undersøgelse afslører radikale rynker i dannelsen af komplekse kulstofmolekyler i rummetDette sammensatte billede viser en illustration af en kulstofrig rød kæmpestjerne (midten), der opvarmer en exoplanet (nederst til venstre) og en overlejring af en nyfundet vej, der kunne gøre det mul
Undersøgelse afslører radikale rynker i dannelsen af komplekse kulstofmolekyler i rummetDette sammensatte billede viser en illustration af en kulstofrig rød kæmpestjerne (midten), der opvarmer en exoplanet (nederst til venstre) og en overlejring af en nyfundet vej, der kunne gøre det mul -
 Kemikere udvikler en ny måde at behandle antibiotika-resistente infektioner påKredit:CC0 Public Domain Med lægemiddelresistente infektioner i stigning og udviklingen af nye antibiotika på tilbagegang, verden kunne bruge en ny strategi i kampen mod stadig mere listige bakt
Kemikere udvikler en ny måde at behandle antibiotika-resistente infektioner påKredit:CC0 Public Domain Med lægemiddelresistente infektioner i stigning og udviklingen af nye antibiotika på tilbagegang, verden kunne bruge en ny strategi i kampen mod stadig mere listige bakt -
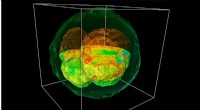 Ny mikroskopteknik afslører indre struktur af levende embryonerEt GLIM billede af et gengivet ko-embryo, der blev skåret gennem midten for at afsløre indre strukturer. Kredit:Billede udlånt af Gabriel Popescu Forskere fra University of Illinois har udviklet e
Ny mikroskopteknik afslører indre struktur af levende embryonerEt GLIM billede af et gengivet ko-embryo, der blev skåret gennem midten for at afsløre indre strukturer. Kredit:Billede udlånt af Gabriel Popescu Forskere fra University of Illinois har udviklet e -
 Hvor meget gryde i den brownie? Chokolade kan afvise testsI denne fredag, 16. august, 2019, Foto, kemiker David Dawson holder et hætteglas op med en ekstraheret chokoladebar, der er inficeret med cannabis, da han demonstrerer test for THC og andre kemikalier
Hvor meget gryde i den brownie? Chokolade kan afvise testsI denne fredag, 16. august, 2019, Foto, kemiker David Dawson holder et hætteglas op med en ekstraheret chokoladebar, der er inficeret med cannabis, da han demonstrerer test for THC og andre kemikalier
- Et frisk pust til længerevarende batterier
- Japansk, Amerikanske astronauter afslutter rumvandring for at reparere robotarm (opdatering)
- Hvad sker der efter lanceringen:To NASA-pædagogiske CubeSats
- Et miljøvenligt batteri lavet af træ (Opdatering)
- Gode steder at finde tomme Aluminium Cans
- Samarbejde konstaterer, at præcisionsnuds mindsker deling af misinformation på begge sider af den …


