Hvad er mere reaktivt sp2 eller sp3 kulstof?
Sp2 kulstof:
- sp2 carboner har en trigonal plan geometri med tre elektronpar arrangeret i en trekantet form omkring carbonatomet.
- Disse kulstoffer har én uhybridiseret p-orbital vinkelret på planet af de tre sp2-orbitaler, hvilket giver mulighed for mere elektrondelokalisering og øget reaktivitet.
- Tilstedeværelsen af p-orbital gør det muligt for sp2-carboner at deltage i forskellige reaktioner såsom elektrofile additioner, nukleofile substitutioner og cycloadditioner.
- Eksempler på sp2-carboner omfatter dem, der findes i alkener, alkyner og aromatiske forbindelser.
Sp3-kulstof:
- sp3 carboner har en tetraedrisk geometri med fire elektronpar arrangeret i en tredimensionel tetraedrisk form omkring carbonatomet.
- Alle fire elektronpar er hybridiseret, hvilket resulterer i fire ækvivalente sp3-orbitaler, der peger mod hjørnerne af et tetraeder.
- Det tetraedriske arrangement af sp3-carboner gør dem mindre reaktive, fordi elektronerne er mere lokaliserede og mindre tilgængelige for reaktioner.
- sp3-carboner findes typisk i mættede forbindelser som alkaner og cycloalkaner, hvor kulstofatomerne er bundet til fire andre atomer.
Sammenfattende er sp2-carboner mere reaktive end sp3-carboner på grund af tilstedeværelsen af den ikke-hybridiserede p-orbital, hvilket giver mulighed for større elektrondelokalisering og letter forskellige kemiske reaktioner.
Sidste artikelHvad er effekten af omrøring på ren eddikesyre?
Næste artikelHvorfor har estere med høj molekylvægt ikke stærke dufte?
 Varme artikler
Varme artikler
-
 Forskere opnår nye resultater i undersøgelsen af uorganiske pigmenter med apatitstrukturPrøve af høj renhed af bariumhypomanganatchlorid. Kredit:Lobachevsky University Forbindelser med apatitstrukturen adskiller sig fra de fleste klasser ved de forskellige kemiske sammensætninger. Fo
Forskere opnår nye resultater i undersøgelsen af uorganiske pigmenter med apatitstrukturPrøve af høj renhed af bariumhypomanganatchlorid. Kredit:Lobachevsky University Forbindelser med apatitstrukturen adskiller sig fra de fleste klasser ved de forskellige kemiske sammensætninger. Fo -
 Video:Hollywood-blodbadenes kemiFalsk blod er en fast bestanddel af Halloween-gyserfilmoplevelsen, men der er ikke én opskrift, der passer til enhver filmskabers behov. Kemien for falsk blod er altid blevet justeret for at skabe den
Video:Hollywood-blodbadenes kemiFalsk blod er en fast bestanddel af Halloween-gyserfilmoplevelsen, men der er ikke én opskrift, der passer til enhver filmskabers behov. Kemien for falsk blod er altid blevet justeret for at skabe den -
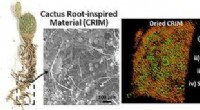 Kaktusrødder inspirerer til skabelse af vandfastholdende materialeKredit:American Chemical Society Under sjældne ørkenregn, kaktusser spilder ingen tid med at suge op og gemme en storms dyrebare nedbør. Inspireret af dette naturfænomen, videnskabsmænd rapportere
Kaktusrødder inspirerer til skabelse af vandfastholdende materialeKredit:American Chemical Society Under sjældne ørkenregn, kaktusser spilder ingen tid med at suge op og gemme en storms dyrebare nedbør. Inspireret af dette naturfænomen, videnskabsmænd rapportere -
 Polymerforskere opdager vej til bæredygtige og bionedbrydelige polyestereOpsætningen af photoredox -polymerisationen i handskerummet med en kold fælde, bestrålet af det blå LED -lys. Kredit:Virginia Tech Der er en god chance for, at du har rørt ved noget, der er lave
Polymerforskere opdager vej til bæredygtige og bionedbrydelige polyestereOpsætningen af photoredox -polymerisationen i handskerummet med en kold fælde, bestrålet af det blå LED -lys. Kredit:Virginia Tech Der er en god chance for, at du har rørt ved noget, der er lave
- Californiens forbrugerbeskyttelseslovgivning kan påvirke virksomheder i hele USA.
- Musik-appen, der hjælper skolebørn med at spille i socialt distancerede orkestre
- Forskere henvender sig til træer for at afgøre, om der eksisterer flercellet liv på exoplaneter
- Kan dine handlinger virkelig redde planeten? Planetarisk regnskab har svaret
- Det tyske kabinet underskriver planer om at tillade kulstoffangst
- Sjælden superleder kan være afgørende for kvanteberegning


