Hvilken type reaktion opstår, når et kemisk stof mister elektroner til et andet stof?
Oxidation er processen med at tabe elektroner, mens reduktion er processen med at få elektroner. Disse processer foregår altid sammen, og kan ikke ske uafhængigt af hinanden.
Redoxreaktioner er vigtige i en lang række kemiske processer, herunder:
* Forbrænding: Når et brændstof brænder, reagerer det med ilt og producerer kuldioxid og vand. I denne reaktion oxideres brændslet, mens ilten reduceres.
* Åndedræt: Når vi trækker vejret, optager vi ilt og bruger det til at nedbryde glukose til energi. I denne reaktion oxideres glukosen, mens ilten reduceres.
* Fotosyntese: Planter bruger sollys til at omdanne kuldioxid og vand til glukose. I denne reaktion reduceres kuldioxiden, mens vandet oxideres.
* Elektrolyse: Når en elektrisk strøm ledes gennem en opløsning af saltvand, spaltes vandet til brint og ilt. I denne reaktion oxideres vandet, mens brinten og ilten reduceres.
Redoxreaktioner er også vigtige i mange industrielle processer, såsom produktion af stål, aluminium og andre metaller.
 Varme artikler
Varme artikler
-
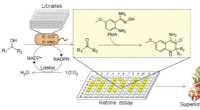 Ny high-throughput screeningsmetode udviklet til ketonerFlowdiagram over PMA-ketonfluorescensscreening. Kredit:Prof. SUN Zhoutongs gruppe Ketoner er af stor betydning som byggesten i syntetisk organisk kemi og biokatalyse. De fleste ketoner kan ikke le
Ny high-throughput screeningsmetode udviklet til ketonerFlowdiagram over PMA-ketonfluorescensscreening. Kredit:Prof. SUN Zhoutongs gruppe Ketoner er af stor betydning som byggesten i syntetisk organisk kemi og biokatalyse. De fleste ketoner kan ikke le -
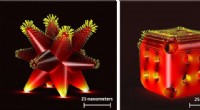 Metalkatalysatorer, der bruges til miljømæssig bæredygtighed, viste sig at nedbrydes og blive min…Nogle af de komplekse strukturelle arrangementer af katalysatorer; venstre er kendt som forgrenet struktur og højre som burstruktur. Kredit:Professor Anna Klinkova fra University of Waterloo Ny fo
Metalkatalysatorer, der bruges til miljømæssig bæredygtighed, viste sig at nedbrydes og blive min…Nogle af de komplekse strukturelle arrangementer af katalysatorer; venstre er kendt som forgrenet struktur og højre som burstruktur. Kredit:Professor Anna Klinkova fra University of Waterloo Ny fo -
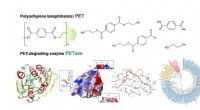 Strukturel indsigt i den molekylære mekanisme ved PET -nedbrydningStrukturel indsigt i den molekylære mekanisme ved poly (ethylenterephthalat) nedbrydning og det fylogenetiske træ af mulige PET -nedbrydende enzymer. Kredit:KAIST Et KAIST metabolisk ingeniørunder
Strukturel indsigt i den molekylære mekanisme ved PET -nedbrydningStrukturel indsigt i den molekylære mekanisme ved poly (ethylenterephthalat) nedbrydning og det fylogenetiske træ af mulige PET -nedbrydende enzymer. Kredit:KAIST Et KAIST metabolisk ingeniørunder -
 Brug af virtual reality-systemer til at undervise i kemi i 3-DEn abstrakt repræsentation af de fodboldformede buckminsterfulleren-molekyler i virtual reality. Kredit:Mike OConnor, i samarbejde med Interactive Scientific Ltd, under CC BY-ND 4.0. Et team af fo
Brug af virtual reality-systemer til at undervise i kemi i 3-DEn abstrakt repræsentation af de fodboldformede buckminsterfulleren-molekyler i virtual reality. Kredit:Mike OConnor, i samarbejde med Interactive Scientific Ltd, under CC BY-ND 4.0. Et team af fo
- Med en stor på vej, jordskælvsalarmsystem lanceres i Oregon
- Husejerskab fører til mindre lykke end forventet
- Interne faktorer, der påvirker Cell Division
- Hvordan 'Dune' blev et fyrtårn for den spæde miljøbevægelse, og en ny økologividenskab
- NASA ser den tropiske storm Jova blive revet fra hinanden
- NASA vælger en mission for at studere solvindens grænse for det ydre solsystem


