Når bly(II)-nitratopløsning tilsættes til kaliumiodid, dannes og forbliver det faste.?
Pb(NO3)2(aq) + 2KI(s) → PbI2(s) + 2KNO3(aq)
Reaktionsprodukterne, bly(II)iodid og kaliumnitrat, er begge opløselige i vand. På grund af bly(II)iodids lave opløselighed udfælder det imidlertid ud af opløsningen og forbliver som et fast stof. Kaliumnitratet forbliver opløst i vandet og danner en farveløs opløsning. Denne reaktion bruges almindeligvis til at teste for tilstedeværelsen af blyioner i en opløsning, da dannelsen af det klare gule bundfald af bly(II)iodid er en klar indikation af tilstedeværelsen af bly.
Sidste artikelHvad er reaktionen mellem dichromat og iodid?
Næste artikelHvordan ligner chlor-37 og calcium-40 hinanden?
 Varme artikler
Varme artikler
-
 Tegn-selv-elektroder sat til at fremskynde udviklingen af mikrodetektionsenhederEn Iron-Man-formet elektrode trykt ved hjælp af teknikken. Kredit:Imperial College London Miniatureanordninger til sansning af biologiske molekyler kunne udvikles hurtigere takket være en hurtig p
Tegn-selv-elektroder sat til at fremskynde udviklingen af mikrodetektionsenhederEn Iron-Man-formet elektrode trykt ved hjælp af teknikken. Kredit:Imperial College London Miniatureanordninger til sansning af biologiske molekyler kunne udvikles hurtigere takket være en hurtig p -
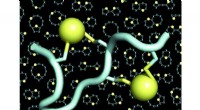 Dobbeltbroede peptider binder ethvert sygdomsmålEn model af et dobbeltbrokoblet peptid (peptidet i lyseblåt, de to broer i gult). Baggrunden for figurerne viser mange eksempler på skeletter (også kaldet stilladser eller rygrade) af dobbeltbroforbun
Dobbeltbroede peptider binder ethvert sygdomsmålEn model af et dobbeltbrokoblet peptid (peptidet i lyseblåt, de to broer i gult). Baggrunden for figurerne viser mange eksempler på skeletter (også kaldet stilladser eller rygrade) af dobbeltbroforbun -
 Ny metode til isolering af tumorceller kan forbedre kræftforskning og -behandlingLeidong Mao (til venstre), en lektor ved UGA College of Engineering arbejdede sammen med ph.d.-studerende Wujun Zhao om at udvikle en ny enhed, der er i stand til at isolere tumorceller. Kredit:Univer
Ny metode til isolering af tumorceller kan forbedre kræftforskning og -behandlingLeidong Mao (til venstre), en lektor ved UGA College of Engineering arbejdede sammen med ph.d.-studerende Wujun Zhao om at udvikle en ny enhed, der er i stand til at isolere tumorceller. Kredit:Univer -
 CRISPR:Mere end blot til genredigering?Den internationale forside af et nyligt nummer af Angewandte Chemie viser billedet fra ECRISPR-forskningen. Kredit: Angewandte Chemie Genredigeringsværktøjet CRISPR er blevet udråbt som et vide
CRISPR:Mere end blot til genredigering?Den internationale forside af et nyligt nummer af Angewandte Chemie viser billedet fra ECRISPR-forskningen. Kredit: Angewandte Chemie Genredigeringsværktøjet CRISPR er blevet udråbt som et vide
- Forskere finder antydninger af israelsk spyware over hele verden
- Sikkerhed og forurening øverst på dagsordenen, når Paris Air Show åbner
- Hvordan et atomangreb på Nordkorea ville bidrage til den globale kræftepidemi
- Nanopartikel-cocktail målretter og dræber tumorer
- Specialiserede væveteknikker muliggør et nyt varmeskjold til planetarisk udforskning
- Sådan hæver du ormme


