Hvad er denne empiriske formel - C5H8NO4?
1. Konverter procenterne til gram:
- Kulstof:52,17% =52,17 g
- Brint:6,90% =6,90 g
- Nitrogen:9,52 % =9,52 g
- Ilt:31,41% =31,41 g
2. Konverter gram af hvert grundstof til mol:
- Kulstof:52,17 g / 12,01 g/mol =4,34 mol
- Brint:6,90 g / 1,01 g/mol =6,84 mol
- Nitrogen:9,52 g / 14,01 g/mol =0,68 mol
- Ilt:31,41 g / 16,00 g/mol =1,96 mol
3. Divider hver molværdi med den mindste molværdi for at få det enkleste hele talforhold:
- Kulstof:4,34 mol / 0,68 mol ≈ 6,4
- Brint:6,84 mol / 0,68 mol ≈ 10,1
- Nitrogen:0,68 mol / 0,68 mol =1
- Ilt:1,96 mol / 0,68 mol ≈ 2,9
4. Afrund forholdet til nærmeste hele tal:
- Kulstof:6
- Brint:10
- Nitrogen:1
- Ilt:3
5. Skriv den empiriske formel ved hjælp af de afrundede forhold:
C6H10NO3
 Varme artikler
Varme artikler
-
 Tager stress ud af resterende stress kortlægningJohn Einhorn (til venstre) og Matt Steiner arbejder med instrumentet Neutron Residual Stress Mapping Facility, strålelinje HB-2B, ved ORNLs High Flux Isotop Reactor. Kredit:ORNL/Genevieve Martin F
Tager stress ud af resterende stress kortlægningJohn Einhorn (til venstre) og Matt Steiner arbejder med instrumentet Neutron Residual Stress Mapping Facility, strålelinje HB-2B, ved ORNLs High Flux Isotop Reactor. Kredit:ORNL/Genevieve Martin F -
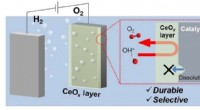 Afskærmning af iltproduktion for at holde brint på vejDen porøse belægning øger holdbarheden af oxygendannende katalysatorer, som industrien ivrigt efterspørger. Kredit:KAUST En porøs ceriumbaseret belægning øger holdbarheden af oxygendannende ka
Afskærmning af iltproduktion for at holde brint på vejDen porøse belægning øger holdbarheden af oxygendannende katalysatorer, som industrien ivrigt efterspørger. Kredit:KAUST En porøs ceriumbaseret belægning øger holdbarheden af oxygendannende ka -
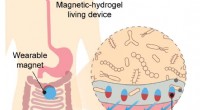 Levende sensorer undersøger tarmens mysterierSkematisk illustration af brugen af levende sensorer indkapslet i en magnetisk hydrogelanordning til undersøgelser af tarmen. Kredit:Xinyue Liu et al Forskning i den menneskelige tarm og mikrobe
Levende sensorer undersøger tarmens mysterierSkematisk illustration af brugen af levende sensorer indkapslet i en magnetisk hydrogelanordning til undersøgelser af tarmen. Kredit:Xinyue Liu et al Forskning i den menneskelige tarm og mikrobe -
 Ny indsigt i dannelsen af bulk metalliske glasKredit:Unsplash/CC0 Public Domain Med evnen til at producere metallisk glas i bulkmængder, den særlige mekaniske opførsel af disse materialer har åbnet op for nye anvendelsesmuligheder. Imidlertid
Ny indsigt i dannelsen af bulk metalliske glasKredit:Unsplash/CC0 Public Domain Med evnen til at producere metallisk glas i bulkmængder, den særlige mekaniske opførsel af disse materialer har åbnet op for nye anvendelsesmuligheder. Imidlertid
- New Zealands White Island vil sandsynligvis bryde ud igen, men et nyt alarmsystem kan give timevis a…
- Adaptiv adfærd, markeder, og hvad det betyder for at helbrede kræft
- Hvordan man opbygger din egen batteripakke AA 9 Volt
- Litteratur kaster lys over Sydhavets historie og mysterium
- Et konsensusdokument om videnskabens tilstand med hensyn til bekæmpelse af misinformation
- Nanoskala DNA-sekventering kunne anspore revolution inden for personlig sundhedspleje


