1,122 g af en ukendt monoprotisk base opløst i 50,0 ml vand titreres til endepunktet med 20,0 en 1,00 M HCL-opløsning?
Trin 1:Beregn antallet af mol HCl brugt i titreringen.
Mol HCl =Koncentration af HCl (M) x Volumen af HCl brugt (L)
Mol HCl =1,00 M x 0,0200 L =0,0200 mol HCl
Trin 2:Da basen er monoprotisk, er antallet af mol base lig med antallet af anvendte mol HCl.
Mol base =mol HCl =0,0200 mol
Trin 3:Beregn molmassen af den ukendte base.
Molær masse af base =masse af base (g) / mol af base (mol)
Masse af base =1,122 g
Mol base =0,0200 mol
Molær masse af base =1,122 g / 0,0200 mol =56,1 g/mol
Derfor er molmassen af den ukendte monoprotiske base 56,1 g/mol.
Sidste artikelHvor rigeligt er grundstoffet kobber på jorden?
Næste artikelHvad er oxidationstallet for fosfor i hvidt fosfor?
 Varme artikler
Varme artikler
-
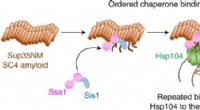 Tre ledsagere koordinerer opdelingen af amyloidfibriller i gærKredit:Yoshiko Nakagawa et al., Nature Chemical Biology (2022). DOI:10.1038/s41589-021-00951-y I et fund, der har vigtige konsekvenser for neurodegenerative lidelser såsom Alzheimers sygdom, har RI
Tre ledsagere koordinerer opdelingen af amyloidfibriller i gærKredit:Yoshiko Nakagawa et al., Nature Chemical Biology (2022). DOI:10.1038/s41589-021-00951-y I et fund, der har vigtige konsekvenser for neurodegenerative lidelser såsom Alzheimers sygdom, har RI -
 Forskeren skaber et kemisk system, der efterligner tidlig celleadfærdSeniorforsker Juan Pérez-Mercader har offentliggjort arbejde om udviklingen af et ur-efterlignende system, der producerer kunstige proto-celler, der vokser, replikere, reagere på lys, og endda udvis
Forskeren skaber et kemisk system, der efterligner tidlig celleadfærdSeniorforsker Juan Pérez-Mercader har offentliggjort arbejde om udviklingen af et ur-efterlignende system, der producerer kunstige proto-celler, der vokser, replikere, reagere på lys, og endda udvis -
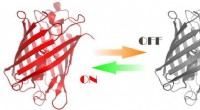 Forskere skabte proteiner styret af lys3D-model af det udviklede protein Kredit:Aleksandr Mishin Forskere har udviklet fluorescerende proteiner, der kan styres af orange og grønt lys. Disse proteiner vil hjælpe med at studere processer
Forskere skabte proteiner styret af lys3D-model af det udviklede protein Kredit:Aleksandr Mishin Forskere har udviklet fluorescerende proteiner, der kan styres af orange og grønt lys. Disse proteiner vil hjælpe med at studere processer -
 En visuel database over humane plasmaforbindelserDatabasen er i stand til at kortlægge sammenhængen mellem de forskellige metabolitter, at tilbyde besøgende yderligere forskningsmuligheder. Kredit:Tohoku Medical Megabank Organization Forskere i
En visuel database over humane plasmaforbindelserDatabasen er i stand til at kortlægge sammenhængen mellem de forskellige metabolitter, at tilbyde besøgende yderligere forskningsmuligheder. Kredit:Tohoku Medical Megabank Organization Forskere i
- Hvad en enkelt bil kan sige om trafikken
- Ny teknik fremskynder produktionen af protein nano-panser
- At forestille sig, hvordan lys opfører sig i 2-D-verdenen, giver forskere indsigt til hurtigere 3-D…
- Hvordan virker lemmerproteser
- Båle raser, mens Californien bager under varmekuppel
- CSI i rummet:Analyse af blodpletmønstre i mikrogravitation


