Hvor mange gram kobber(II)sulfatpentahydrat skal du måle for at have 10,0 vandfrit kobber(II)sulfat?
- Kobber(II)sulfatpentahydrat har formlen CuSO4.5H2O og en molær masse på ca. 249,69 g/mol.
- Vandfrit kobber(II)sulfat har formlen CuSO4 og en molær masse på cirka 159,61 g/mol.
Omdannelsen kan sættes op som en andel baseret på molforholdet mellem forbindelserne:
(Masse af CuSO4.5H2O) / (Molar masse af CuSO4.5H2O) =(Masse af CuSO4) / (Molar masse af CuSO4)
Omarrangering af ligningen for at løse massen af CuSO4.5H2O:
(Masse af CuSO4.5H2O) =(Masse af CuSO4) × (Molar masse af CuSO4.5H2O) / (Molar masse af CuSO4)
Tilslut værdierne:
(Masse af CuSO4.5H2O) =10,0 g × (249,69 g/mol) / (159,61 g/mol)
Beregning af resultatet:
(Masse af CuSO4.5H2O) ≈ 15,63 g
Derfor skal du bruge cirka 15,63 gram kobber(II)sulfatpentahydrat for at opnå 10,0 gram vandfrit kobber(II)sulfat.
Sidste artikelEr Inconel kompatibel med saltsyre?
Næste artikelHvorfor er natrium og klor ikke stabile grundstoffer?
 Varme artikler
Varme artikler
-
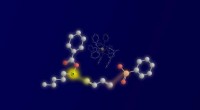 Forskere bruger ketylradikaler til en ny flerkomponentreaktionDe tre reaktanter og deres binding:radikal af ketyltypen til venstre, 1,3-dien i midten og nukleofil sulfinat til højre. De reaktive atomer og bindingen, der dannes, er fremhævet med gult (ketylkulsto
Forskere bruger ketylradikaler til en ny flerkomponentreaktionDe tre reaktanter og deres binding:radikal af ketyltypen til venstre, 1,3-dien i midten og nukleofil sulfinat til højre. De reaktive atomer og bindingen, der dannes, er fremhævet med gult (ketylkulsto -
 Spild ikke, vil ikke:en hjemmelavet plan om at gøre plast og dæk til brændstofKredit:Monash University Reducere, genbruge, genbruge. Som at børste tænder efter et måltid, genbrug er bare det rigtige at gøre. Men nu hvor Kina er holdt op med at tage vores skraldespand, vi k
Spild ikke, vil ikke:en hjemmelavet plan om at gøre plast og dæk til brændstofKredit:Monash University Reducere, genbruge, genbruge. Som at børste tænder efter et måltid, genbrug er bare det rigtige at gøre. Men nu hvor Kina er holdt op med at tage vores skraldespand, vi k -
 Forskere tager røntgenbilleder af elektriske køretøjers batterier, efterhånden som de nedbrydes …Toby Bond justerer en batteriprøve på BMIT-strålelinjen. Kredit:Canadian Light Source Canadian Light Source (CLS) forsker Toby Bond bruger røntgenstråler til at hjælpe med at konstruere kraftfulde
Forskere tager røntgenbilleder af elektriske køretøjers batterier, efterhånden som de nedbrydes …Toby Bond justerer en batteriprøve på BMIT-strålelinjen. Kredit:Canadian Light Source Canadian Light Source (CLS) forsker Toby Bond bruger røntgenstråler til at hjælpe med at konstruere kraftfulde -
 Brug af matematik til at forudsige SARS-CoV-2-proteinmutationerEt team af forskere brugte matematik til at forudsige, hvilke områder af SARS-CoV-2 spike-proteinet der er mest tilbøjelige til at mutere. Kredit:Jill Hemman/ORNL, U.S.A. Dept. of Energy Oak Ridge
Brug af matematik til at forudsige SARS-CoV-2-proteinmutationerEt team af forskere brugte matematik til at forudsige, hvilke områder af SARS-CoV-2 spike-proteinet der er mest tilbøjelige til at mutere. Kredit:Jill Hemman/ORNL, U.S.A. Dept. of Energy Oak Ridge
- Regnorme - integrerede økosystemingeniører
- Små magnetiske DNA-partikler beskytter olivenolie mod falskmøntnere
- Safirer og rubiner på himlen
- Opladning af biler derhjemme om natten er ikke vejen at gå, viser undersøgelse
- Den egyptiske domstol dømmer Uber, Careem ulovligt; klage forventes
- Hvad er forskellene mellem evolutionsteori og modstridende teorier?


