Hvad ville der ske, hvis du forsøger at nedbryde en prøve af svovl?
At nedbryde en prøve af svovl ville involvere at adskille atomerne fra hinanden. Svovlatomer er stærkt bundet sammen af kovalente bindinger, som er kemiske bindinger dannet ved deling af elektronpar mellem to atomer. For at bryde disse bindinger skal der tilføres energi i form af varme eller lys.
Hvis en prøve af svovl opvarmes til en tilstrækkelig høj temperatur, vil de kovalente bindinger mellem svovlatomerne bryde, og atomerne bliver til frie radikaler. Frie radikaler er meget reaktive atomer eller molekyler med uparrede elektroner, hvilket betyder, at de mangler en elektron fra deres ydre skal.
De frie radikalers svovlatomer kan derefter reagere med andre molekyler i miljøet, såsom oxygen eller brint, og danne nye forbindelser. For eksempel, hvis svovlatomerne kommer i kontakt med ilt, vil de reagere og danne svovldioxid (SO2), en skarp, irriterende gas.
Sammenfattende, hvis du forsøger at nedbryde en prøve af svovl, vil den adskilles i frie radikaler svovlatomer, som derefter kan reagere med andre molekyler i miljøet og danne nye forbindelser.
 Varme artikler
Varme artikler
-
 Naturlig mineralsk hackmanit demonstrerer meget gentagelig farveændringsevneHackmanit bliver lilla under UV-bestråling, og farven falmer tilbage til hvid på få minutter under almindeligt hvidt lys. Denne prøve er fra Grønland. Kredit:Mika Lastusaari Mens de undersøgte hack
Naturlig mineralsk hackmanit demonstrerer meget gentagelig farveændringsevneHackmanit bliver lilla under UV-bestråling, og farven falmer tilbage til hvid på få minutter under almindeligt hvidt lys. Denne prøve er fra Grønland. Kredit:Mika Lastusaari Mens de undersøgte hack -
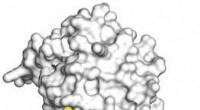 Krystalstruktur afslører, hvordan curcumin hæmmer kræftEt 3D billede, opnået ved hjælp af røntgenkrystallografi, viser curcumin i gul og rød binding til kinase-enzym dual-specificity tyrosin-reguleret kinase 2 (DYRK2) i hvidt på atomniveau. Kredit:UC San
Krystalstruktur afslører, hvordan curcumin hæmmer kræftEt 3D billede, opnået ved hjælp af røntgenkrystallografi, viser curcumin i gul og rød binding til kinase-enzym dual-specificity tyrosin-reguleret kinase 2 (DYRK2) i hvidt på atomniveau. Kredit:UC San -
 Avanceret mikroskopi afslører usædvanlig DNA-strukturAdam Backer, en optisk videnskabsmand ved Sandia National Laboratories, hjulpet med at udvikle en avanceret mikroskopiteknik, der afslørede stærkt hældende basepar i en strakt form af DNA. Kredit:Rand
Avanceret mikroskopi afslører usædvanlig DNA-strukturAdam Backer, en optisk videnskabsmand ved Sandia National Laboratories, hjulpet med at udvikle en avanceret mikroskopiteknik, der afslørede stærkt hældende basepar i en strakt form af DNA. Kredit:Rand -
 Ferroelektriske selvsamlede molekylære materialerDet første materiale med konduktivitetsegenskaber, der kan tændes og slukkes ved hjælp af ferroelektrisk polarisering. Kredit:Thor Balkhed Professor Martijn Kemerink fra Linköping Universitet har
Ferroelektriske selvsamlede molekylære materialerDet første materiale med konduktivitetsegenskaber, der kan tændes og slukkes ved hjælp af ferroelektrisk polarisering. Kredit:Thor Balkhed Professor Martijn Kemerink fra Linköping Universitet har
- Et spørgsmål om tyngdekraft - at forstå, hvordan planter vokser i rummet
- Er for alle grundstoffer den mindste partikel, der kan eksistere uafhængigt, et atom?
- Rusland gennemfører den første Soyuz -lancering siden ulykken
- Introduktion af den største kvantefotoniske processor til dato
- Ny enhed kan øge batterilevetiden for elektroniske enheder mere end hundrede gange
- Sådan beregnes en vandret tangenslinje


