Hvorfor er smeltepunktet for p-chlorphenol højere end o-chlorphenol?
I para-chlorphenol er hydroxylgruppen og chloratomet placeret på modsatte sider af benzenringen. Dette gør det muligt for hydroxylgrupperne i tilstødende molekyler at danne hydrogenbindinger mere effektivt, hvilket resulterer i stærkere intermolekylære interaktioner og et højere smeltepunkt.
På den anden side, i ortho-chlorphenol, støder hydroxylgruppen og chloratomet op til hinanden. Denne steriske hindring hindrer dannelsen af intermolekylære hydrogenbindinger, hvilket svækker de intermolekylære interaktioner. Som et resultat har ortho-chlorphenol et lavere smeltepunkt sammenlignet med para-chlorphenol.
Sidste artikelHvilken type kemisk binding har CH4?
Næste artikelHvordan afbalancerer du kemikalierne i Bor og H2O?
 Varme artikler
Varme artikler
-
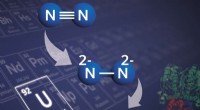 En uranbaseret forbindelse forbedrer fremstillingen af nitrogenprodukterEn illustration af, hvordan den uranbaserede forbindelse, der blev udviklet i denne undersøgelse, ville fungere. Kredit:Marinella Mazzanti/EPFL Kvælstof er rigeligt tilgængelig i naturen og danner
En uranbaseret forbindelse forbedrer fremstillingen af nitrogenprodukterEn illustration af, hvordan den uranbaserede forbindelse, der blev udviklet i denne undersøgelse, ville fungere. Kredit:Marinella Mazzanti/EPFL Kvælstof er rigeligt tilgængelig i naturen og danner -
 Kumarinforbindelser fra egetræsfade kunne bidrage til bitter smag i vin og spiritusKredit:Pixabay/CC0 Public Domain Vin og spiritus er komplekse blandinger af smags- og aromaforbindelser, hvoraf nogle opstår under lagring i træfade. Blandt andre forbindelser, egetræ frigiver kum
Kumarinforbindelser fra egetræsfade kunne bidrage til bitter smag i vin og spiritusKredit:Pixabay/CC0 Public Domain Vin og spiritus er komplekse blandinger af smags- og aromaforbindelser, hvoraf nogle opstår under lagring i træfade. Blandt andre forbindelser, egetræ frigiver kum -
 Tellurium gør forskellenProfessor Wolfgang Weigand fra det tyske universitet i Jena viser usædvanlige strukturer af tellurforbindelser. Kredit:Anne Günther/Uni Jena Det periodiske system indeholder 118 kemiske grundstoff
Tellurium gør forskellenProfessor Wolfgang Weigand fra det tyske universitet i Jena viser usædvanlige strukturer af tellurforbindelser. Kredit:Anne Günther/Uni Jena Det periodiske system indeholder 118 kemiske grundstoff -
 Design og genanvendelse af celleceptorerTegneserie, der illustrerer beregningsmæssig manipulation af langtrækkende signaloverførsel i celleceptorer. Kredit:Daniel Keri, EPFL EPFL -forskere har udviklet en beregningsmetode til modellerin
Design og genanvendelse af celleceptorerTegneserie, der illustrerer beregningsmæssig manipulation af langtrækkende signaloverførsel i celleceptorer. Kredit:Daniel Keri, EPFL EPFL -forskere har udviklet en beregningsmetode til modellerin
- Forskeren skaber teknik til nanoskala målinger ved hjælp af lys
- Bioprocesingeniører genvinder glucosinolat fra oliefrømel
- Er en basisindkomst løsningen på vedvarende uligheder, som kvinder står over for?
- Med 66 millioner mennesker, der lever uden ordentlig bolig, hvad kan arkitekter gøre?
- Forskere søger nye måder at forbedre kommunikationen om jordskælvsrisiko
- Hvordan vi bygger verdens største optiske teleskop for at knække nogle af de største gåder inden…


