Hvordan bliver et atom af rubidium-85 til en rubidiumion med 1 ladning?
Specifikt i tilfælde af rubidium-85 har den i alt 37 elektroner. I sin neutrale tilstand er antallet af positivt ladede protoner i dens kerne afbalanceret af de 37 negativt ladede elektroner. For at blive en ion med 1 ladning skal den miste en elektron, så den efterlades med 36 elektroner og 37 protoner. Da antallet af protoner nu overstiger antallet af elektroner med én, har atomet en netto positiv ladning på +1, hvilket gør det til en rubidium-85 ion.
Denne proces med at miste en elektron er typisk resultatet af kemiske reaktioner eller interaktioner med eksterne energikilder, såsom varme eller lys, som giver nok energi til at overvinde den tiltrækningskraft, der er mellem elektronen og den positivt ladede kerne.
 Varme artikler
Varme artikler
-
 Forskere udvikler levedygtige, miljøvenligt alternativ til StyrofoamEn miljøvenlig, plantebaseret materiale, der for første gang fungerer bedre end Styrofoam til isolering. Kredit:WSU Washington State University forskere har udviklet en miljøvenlig, plantebaseret
Forskere udvikler levedygtige, miljøvenligt alternativ til StyrofoamEn miljøvenlig, plantebaseret materiale, der for første gang fungerer bedre end Styrofoam til isolering. Kredit:WSU Washington State University forskere har udviklet en miljøvenlig, plantebaseret -
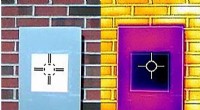 Den hvideste maling er her - og den er den sejeste. Bogstaveligt talt.Et infrarødt kamera viser, hvordan en prøve af den hvideste hvide maling (den mørke lilla firkant i midten) faktisk afkøler brættet under omgivelsestemperatur, noget, som ikke engang kommercielle varm
Den hvideste maling er her - og den er den sejeste. Bogstaveligt talt.Et infrarødt kamera viser, hvordan en prøve af den hvideste hvide maling (den mørke lilla firkant i midten) faktisk afkøler brættet under omgivelsestemperatur, noget, som ikke engang kommercielle varm -
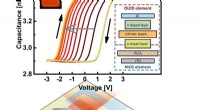 pinMOS:Ny hukommelsesenhed kan skrives på og udlæses optisk eller elektriskPinMOS-hukommelsen - en organisk halvlederenhed, der er et resultat af kombinationen af en OLED og en kondensator. Det har egenskaberne af en Memcapacitor, interagerer med lys og kan skrives og slet
pinMOS:Ny hukommelsesenhed kan skrives på og udlæses optisk eller elektriskPinMOS-hukommelsen - en organisk halvlederenhed, der er et resultat af kombinationen af en OLED og en kondensator. Det har egenskaberne af en Memcapacitor, interagerer med lys og kan skrives og slet -
 Kul afslører en sofistikeret side:Beskidt kulstof kan bruges til at lave en række nyttige enhederInfrarødt (varme) billede viser en varmeanordning lavet af dampknækket tjære, udglødet med laser, som blev formet til et MIT-logo for at demonstrere processens kontrollerbarhed. Kredit:Massachusetts I
Kul afslører en sofistikeret side:Beskidt kulstof kan bruges til at lave en række nyttige enhederInfrarødt (varme) billede viser en varmeanordning lavet af dampknækket tjære, udglødet med laser, som blev formet til et MIT-logo for at demonstrere processens kontrollerbarhed. Kredit:Massachusetts I
- Forskere udvider forståelsen af, hvordan DNA er organiseret
- Udrede hemmelighederne bag orme- og edderkoppesilke
- Astronomer opdager nye massive stjerner i den unge hob VVV CL074
- Fra 3-D til 2-D og tilbage:reversibel omdannelse af lipidkugler til ultratynde ark
- Nyt design til længerevarende nattesynskameraer
- Oversættelse (biologi): Definition, trin, diagram


