Hvad sker der, når saltsyre blandes med aluminiumsfolie?
2Al(s) + 6HCl(aq) → 2AlCl3(aq) + 3H2(g)
I denne reaktion mister aluminiumsatomer tre elektroner til hydrogenatomer og danner Al3+ ioner og H2-molekyler. Al3+-ionerne kombineres derefter med Cl-ioner fra HCl for at danne aluminiumchlorid.
Reaktionen mellem HCl og aluminiumsfolie er eksoterm, hvilket betyder, at den frigiver varme. Brintgassen, der produceres under reaktionen, er brandfarlig og kan brænde, hvis den antændes.
For at undgå potentielle farer er det vigtigt at håndtere saltsyre og aluminiumsfolie med forsigtighed. Bær altid handsker og øjenværn, når du arbejder med disse materialer, og sørg for, at eksperimentet udføres i et godt ventileret område.
Sidste artikelMedfører brud på et spejl ændringer i de kemiske egenskaber?
Næste artikelIndeholder syrer H-gruppen?
 Varme artikler
Varme artikler
-
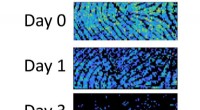 Rester i fingeraftryk indeholder spor af deres alderNiveauer af umættet triacylglycerol falder i fingeraftryk fra et individ fra dag 0 (øverst) til dag 1 (midten) og dag 3 (nederst). Kredit:Tilpasset fra Analytisk kemi 2020, DOI:10.1021/acs.analchem.
Rester i fingeraftryk indeholder spor af deres alderNiveauer af umættet triacylglycerol falder i fingeraftryk fra et individ fra dag 0 (øverst) til dag 1 (midten) og dag 3 (nederst). Kredit:Tilpasset fra Analytisk kemi 2020, DOI:10.1021/acs.analchem. -
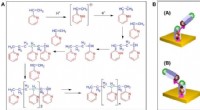 Oprettelse af en chiral polymer ud fra achirale monomerer ved hjælp af et magnetfeltSkematisk og en foreslået mekanisme for elektropolymerisationsprocessen af 2-vinylpyridin. (A) Skematisk over elektropolymerisationsprocessen af 2-vinylpyridin (25). (B) Skematisk af en foreslået
Oprettelse af en chiral polymer ud fra achirale monomerer ved hjælp af et magnetfeltSkematisk og en foreslået mekanisme for elektropolymerisationsprocessen af 2-vinylpyridin. (A) Skematisk over elektropolymerisationsprocessen af 2-vinylpyridin (25). (B) Skematisk af en foreslået -
 Ny metode udviklet til at udvinde antibiotikarester i fødevarer fra animalske kilderDen forsker, der er ansvarlig for undersøgelsen, Soledad González, i laboratoriet Kredit:University of Córdoba Coccidiose er en slags tarmsygdom, der rammer forskellige grupper af dyr. Det hæmmer
Ny metode udviklet til at udvinde antibiotikarester i fødevarer fra animalske kilderDen forsker, der er ansvarlig for undersøgelsen, Soledad González, i laboratoriet Kredit:University of Córdoba Coccidiose er en slags tarmsygdom, der rammer forskellige grupper af dyr. Det hæmmer -
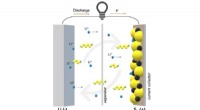 Forskere sætter opløsningen i opløsningsmiddel til lithium-svovl batteriudfordringDette diagram viser et lithium-svovlbatteri under afladning. Forskere var i stand til at observere, hvordan en bestemt type elektrolytmateriale kan reducere pendlingen af polysulfidforbindelser (vis
Forskere sætter opløsningen i opløsningsmiddel til lithium-svovl batteriudfordringDette diagram viser et lithium-svovlbatteri under afladning. Forskere var i stand til at observere, hvordan en bestemt type elektrolytmateriale kan reducere pendlingen af polysulfidforbindelser (vis
- Større, dyrere iPhone forventes til Apple -arrangement onsdag
- Forskere tester curcumin nanoemulsion til behandling af tarmbetændelse
- Klimaændringer øger forekomsten af skadelige parasitter, advare videnskabsmænd
- Ocean Tide Experiment
- Egypten skal være vært for Huaweis første MENA-skyplatform:Cairo
- Usædvanlig alliance for at redde blåhvaler, der er gået i stå af Sri Lanka


