Hvilken grundstofgruppe er bedst kendt for at binde med en kovalent binding?
 Varme artikler
Varme artikler
-
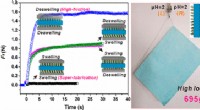
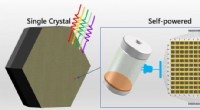 Multi-tommer enkelt-krystallinsk perovskit til selvforsynet integreret kredsløb fotodetektion rappo…Tommerstørrelse perovskit-enkeltkrystaller af høj kvalitet dannet ved at undertrykke faseadskillelsen til applikationer i lysdrevne integrerede kredsløb. Kredit:DICP Perovskitter med flere katione
Multi-tommer enkelt-krystallinsk perovskit til selvforsynet integreret kredsløb fotodetektion rappo…Tommerstørrelse perovskit-enkeltkrystaller af høj kvalitet dannet ved at undertrykke faseadskillelsen til applikationer i lysdrevne integrerede kredsløb. Kredit:DICP Perovskitter med flere katione -
 Hvordan vand hjælper substratet ind i enzymetKredit:Pixabay/CC0 Public Domain Forskere fra Bochum og Berkeley har undersøgt, hvorfor bure kan øge den katalytiske aktivitet af lukkede molekyler. Ved at bruge terahertz-spektroskopi og kompleks
Hvordan vand hjælper substratet ind i enzymetKredit:Pixabay/CC0 Public Domain Forskere fra Bochum og Berkeley har undersøgt, hvorfor bure kan øge den katalytiske aktivitet af lukkede molekyler. Ved at bruge terahertz-spektroskopi og kompleks -
 Syntetisk tosidet gekkoerfod kunne muliggøre undervandsrobotikKredit:American Chemical Society Gekkoer er velkendte for ubesværet at klatre op ad vægge og på hovedet over lofter. Selv i glatte regnskove, firbenene bevarer deres greb. Nu har forskere skabt et
Syntetisk tosidet gekkoerfod kunne muliggøre undervandsrobotikKredit:American Chemical Society Gekkoer er velkendte for ubesværet at klatre op ad vægge og på hovedet over lofter. Selv i glatte regnskove, firbenene bevarer deres greb. Nu har forskere skabt et -
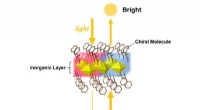 Nyt magnetdesign med spejllignende egenskaberDen magiske spejllignende magnet. Lysstyrken af det transmitterede lys fra magneten ændrer sig alt efter om materialet ses forfra eller bagfra. Kredit:Kouji Taniguchi Forskere ved Tohoku Univers
Nyt magnetdesign med spejllignende egenskaberDen magiske spejllignende magnet. Lysstyrken af det transmitterede lys fra magneten ændrer sig alt efter om materialet ses forfra eller bagfra. Kredit:Kouji Taniguchi Forskere ved Tohoku Univers
- Kan savanne dukke op i de kolde høje breddegrader og højder på grund af igangværende hurtig opva…
- Undersøgelse:De fleste amerikanere mener ikke, at mindre diskrimination mod sorte betyder mere mod …
- Kemikere udvikler nanokatalysatorer til kontinuerlig biobrændstofsyntese
- Trafikprop på Everest, da yderligere to klatrere dør ved at nå toppen
- Brug af let turbulens til at generere frekvenskamme fra små ringlasere
- Under solformørkelsen i 2024 vil texanere støtte en national forskningsindsats for at studere sole…


