Hvad er det maksimale antal atomer, der kan bindes i en hydrogenbinding?
Sidste artikelHvad er krystalstrukturen af svovl?
Næste artikelHvad er klassificeringen af platin?
 Varme artikler
Varme artikler
-
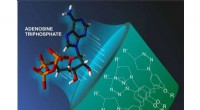 Fælder for energikildemolekyler i cellerKredit:Natalia Deryugina Et team af forskere, inklusive en RUDN-kemiker, har syntetiseret nye molekyler, der tilhører klassen af calixarener, skållignende hule strukturer. Disse stoffer ser ud t
Fælder for energikildemolekyler i cellerKredit:Natalia Deryugina Et team af forskere, inklusive en RUDN-kemiker, har syntetiseret nye molekyler, der tilhører klassen af calixarener, skållignende hule strukturer. Disse stoffer ser ud t -
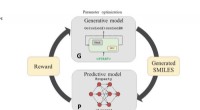 Kunstigt intelligenssystem designer medicin fra bundenWorkflowet af dyb RL-algoritme til generering af nye SMILES-strenge af forbindelser med de ønskede egenskaber. (A) Træningstrin i den generative Stack-RNN. (B) Generatortrin for den generative Stack-R
Kunstigt intelligenssystem designer medicin fra bundenWorkflowet af dyb RL-algoritme til generering af nye SMILES-strenge af forbindelser med de ønskede egenskaber. (A) Træningstrin i den generative Stack-RNN. (B) Generatortrin for den generative Stack-R -
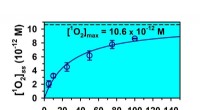 Omdannelse af absorberede fotoner med 2-oxocarboxylsyrer til yderst reaktivt singlet oxygenHøj steady-state singlet iltproduktion, [1O2]ss, under en times bestråling af luftmættede opløsninger af pyruvinsyre i vand. Kredit:Marcelo I. Guzman Forskere ved University of Kentucky fandt ud a
Omdannelse af absorberede fotoner med 2-oxocarboxylsyrer til yderst reaktivt singlet oxygenHøj steady-state singlet iltproduktion, [1O2]ss, under en times bestråling af luftmættede opløsninger af pyruvinsyre i vand. Kredit:Marcelo I. Guzman Forskere ved University of Kentucky fandt ud a -
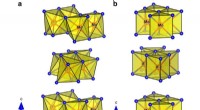 En ny metode til at udvinde brint fra vand mere effektivt for at opfange vedvarende energiKrystalstruktur og {MoTe}6 polyedre, der viser byggestenene i hver polymorf. en monoklinisk 1T′-MoTe2-fase og b hexagonal 2H-MoTe2-fase. Kredit: Naturkommunikation 10.1038/s41467-019-12831-0 En n
En ny metode til at udvinde brint fra vand mere effektivt for at opfange vedvarende energiKrystalstruktur og {MoTe}6 polyedre, der viser byggestenene i hver polymorf. en monoklinisk 1T′-MoTe2-fase og b hexagonal 2H-MoTe2-fase. Kredit: Naturkommunikation 10.1038/s41467-019-12831-0 En n
- Farvel Cassini:Saturn -rumfartøjer gør ild, sidste dyk (opdatering)
- Polaron-grænsefladeentropi som en vej til høj termoelektrisk ydeevne i DAE-dopet PEDOT:PSS-film
- Astronomer opdager den mest massive neutronstjerne, der nogensinde er målt
- "Unifix Cubes Activities
- Kvinder genererer lavere rejserelaterede drivhusgasemissioner, undersøgelse finder
- Hvad er forskellen mellem en Centriole & a Centrosome?


