Har en syre med en pH på 1 eller 3 større H-koncentration?
pH-værdien af en opløsning er et mål for dens surhed eller basicitet og defineres som den negative logaritme af hydrogenionkoncentrationen ([H+]). Jo lavere pH, jo højere [H+], og omvendt.
En pH på 1 betyder, at [H+] er 10^-1 =0,1 M. En pH på 3 betyder, at [H+] er 10^-3 =0,001 M.
Derfor har en syre med en pH på 1 en større [H+] og er derfor mere sur end en syre med en pH på 3.
 Varme artikler
Varme artikler
-
 Brug af kunstig intelligens til at lugte roserneAnandasankar Ray er professor i molekylær, celle- og systembiologi ved UC Riverside. Kredit:L. Duka. Et par forskere ved University of California, Riverside, har brugt maskinlæring til at forstå,
Brug af kunstig intelligens til at lugte roserneAnandasankar Ray er professor i molekylær, celle- og systembiologi ved UC Riverside. Kredit:L. Duka. Et par forskere ved University of California, Riverside, har brugt maskinlæring til at forstå, -
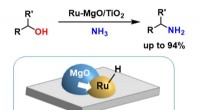 En forbedret ruthenium-baseret katalysator til primær aminsynteseDirekte aminering af alkoholer over Ru-MgO/TiO2 aktiveret ved elektrondonation fra MgO. Kredit:Yusuke Kita Forskere ved Tokyo Institute of Technology (Tokyo Tech) har udviklet en højtydende genanv
En forbedret ruthenium-baseret katalysator til primær aminsynteseDirekte aminering af alkoholer over Ru-MgO/TiO2 aktiveret ved elektrondonation fra MgO. Kredit:Yusuke Kita Forskere ved Tokyo Institute of Technology (Tokyo Tech) har udviklet en højtydende genanv -
 Undersøgelse af bedre biotransformationerMadagaskar periwinkle. Kredit:Wikimedia Commons, CC BY-SA Forskning i International Journal of Bioinformatics Research and Applications har undersøgt kemien og opførselen af et nyttigt naturprodu
Undersøgelse af bedre biotransformationerMadagaskar periwinkle. Kredit:Wikimedia Commons, CC BY-SA Forskning i International Journal of Bioinformatics Research and Applications har undersøgt kemien og opførselen af et nyttigt naturprodu -
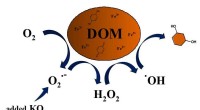 Superoxid producerer hydroxylradikaler, der nedbryder opløst organisk stof i vandSuperoxid kan drive autokatalytisk produktion af hydroxylradikaler i nærværelse af komplekser af naturligt opløst organisk stof og jern. I autokatalyse, hydroxylradikaler omdanner muligvis aromatiske
Superoxid producerer hydroxylradikaler, der nedbryder opløst organisk stof i vandSuperoxid kan drive autokatalytisk produktion af hydroxylradikaler i nærværelse af komplekser af naturligt opløst organisk stof og jern. I autokatalyse, hydroxylradikaler omdanner muligvis aromatiske
- En klasse for sig:Nye faktorer styrer transport af rødalger kloroplastprotein
- Forskere udvikler fleksibel plastisk magnetisk hukommelsesenhed
- Gør drømme til virkelighed:Gør grafen af plast?
- Heres, hvorfor din telefon stopper med at arbejde i Cold
- Første påvisning af regn over havet af navigationssatellitter
- Internettet har gjort meget, men indtil videre lidt for økonomisk vækst


