Er et diatomisk molekyle mere tilbøjelige til at blive holdt sammen af en kovalent binding eller ionbinding?
Ionbindinger dannes, når et atom overfører elektroner til et andet atom, hvilket skaber to modsat ladede ioner. Kovalente bindinger dannes, når to atomer deler elektroner, hvilket skaber et molekyle med en stabil elektronkonfiguration.
I et diatomisk molekyle er de to atomer normalt meget tæt på hinanden, og deres atomare orbitaler overlapper hinanden betydeligt. Dette giver mulighed for deling af elektroner mellem atomerne, hvilket er det, der danner en kovalent binding.
Ionbindinger er mindre tilbøjelige til at dannes mellem to atomer, der er meget tæt på hinanden, fordi den stærke frastødning mellem de positivt og negativt ladede ioner ville destabilisere molekylet.
Derfor er det mere sandsynligt, at et diatomisk molekyle holdes sammen af en kovalent binding end en ionbinding.
Sidste artikelPilen i en kemisk ligning læses som en?
Næste artikelEr følgende ligning balanceret CS2 plus 2Cl2 CCl4 S2Cl2?
 Varme artikler
Varme artikler
-
 Forskere fastlægger destination for protein, der leverer zinkNærbillede af en prøveplade fyldt med gærcellekulturer brugt i disse undersøgelser. Disse plader giver forskere mulighed for at køre eksperimenter på mange duplikatprøver samtidigt for at øge tilliden
Forskere fastlægger destination for protein, der leverer zinkNærbillede af en prøveplade fyldt med gærcellekulturer brugt i disse undersøgelser. Disse plader giver forskere mulighed for at køre eksperimenter på mange duplikatprøver samtidigt for at øge tilliden -
 Ny mikroskopi virker ved ekstrem varme, kaster lys over legeringer til atomreaktorerAfsaneh Rabiei er her afbilledet med den enhed, hun udviklede, der kan fange scanning elektronmikroskopi (SEM) billeder i realtid ved temperaturer op til 1, 000 grader Celsius, mens der påføres spændi
Ny mikroskopi virker ved ekstrem varme, kaster lys over legeringer til atomreaktorerAfsaneh Rabiei er her afbilledet med den enhed, hun udviklede, der kan fange scanning elektronmikroskopi (SEM) billeder i realtid ved temperaturer op til 1, 000 grader Celsius, mens der påføres spændi -
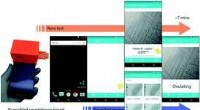 Forskere udvikler smartphone-baseret ægløsningstestKredit: Lab on a Chip (2018). DOI:10.1039/C8LC00792F Efterforskere fra Brigham and Womens Hospital er ved at udvikle en automatiseret, lavprisværktøj til at forudsige en kvindes ægløsning og hjæl
Forskere udvikler smartphone-baseret ægløsningstestKredit: Lab on a Chip (2018). DOI:10.1039/C8LC00792F Efterforskere fra Brigham and Womens Hospital er ved at udvikle en automatiseret, lavprisværktøj til at forudsige en kvindes ægløsning og hjæl -
 Kan du lave en 10-årig maltwhisky på uger? Kemien siger jaVille du stadig være villig til at vente på whisky? Kredit:Shutterstock.com I løbet af de sidste par år er whisky-drikkende verden blevet introduceret til adskillige nye produkter, der hævder at p
Kan du lave en 10-årig maltwhisky på uger? Kemien siger jaVille du stadig være villig til at vente på whisky? Kredit:Shutterstock.com I løbet af de sidste par år er whisky-drikkende verden blevet introduceret til adskillige nye produkter, der hævder at p


