Hvad er antallet af atomer i 20,5 g sølv?
1. Bestem den molære masse af sølv (Ag). Den molære masse af Ag er 107,868 g/mol.
2. Beregn antallet af mol Ag i 20,5 g.
Antal mol =masse / molær masse
=20,5 g / 107,868 g/mol
=0,1898 mol
3. Brug Avogadros tal til at bestemme antallet af atomer i 0,1898 mol Ag. Avogadros tal er 6,022 x 10^23 atomer/mol.
Antal atomer =antal mol × Avogadros tal
=0,1898 mol × 6,022 x 10^23 atomer/mol
=1,143 x 10^23 atomer
Derfor er der cirka 1,143 x 10^23 atomer i 20,5 g sølv.
Sidste artikelEr jod bliver en lilla gas kemisk ændring?
Næste artikelHvordan omdannes gas fra væske til form i gasflaske?
 Varme artikler
Varme artikler
-
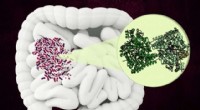 Bakterielt enzym kan blive et nyt mål for antibiotikaMIT-forskere har opdaget strukturen af et usædvanligt enzym, som nogle mikrober bruger til at nedbryde en komponent af kollagen i den menneskelige tarm. Kredit:Christine Daniloff, MIT MIT og Har
Bakterielt enzym kan blive et nyt mål for antibiotikaMIT-forskere har opdaget strukturen af et usædvanligt enzym, som nogle mikrober bruger til at nedbryde en komponent af kollagen i den menneskelige tarm. Kredit:Christine Daniloff, MIT MIT og Har -
 Ny tilgang gør det letteste bilmetal mere økonomisk, nyttigEt rør med en diameter på 50 mm med en vægtykkelse på 1,5 mm skabt af en solid luns magnesiumlegering ved hjælp af PNNLs ShAPE™-ekstruderingsproces. Kredit:PNNL Magnesium - det letteste af alle st
Ny tilgang gør det letteste bilmetal mere økonomisk, nyttigEt rør med en diameter på 50 mm med en vægtykkelse på 1,5 mm skabt af en solid luns magnesiumlegering ved hjælp af PNNLs ShAPE™-ekstruderingsproces. Kredit:PNNL Magnesium - det letteste af alle st -
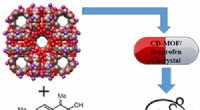 Længerevarende smertelindring med MOF'erKredit:American Chemical Society Til behandling af hovedpine, rygsmerter eller feber, de fleste af os har nået ibuprofen på et eller andet tidspunkt. Men vi skal ofte tage doser hver fjerde til sj
Længerevarende smertelindring med MOF'erKredit:American Chemical Society Til behandling af hovedpine, rygsmerter eller feber, de fleste af os har nået ibuprofen på et eller andet tidspunkt. Men vi skal ofte tage doser hver fjerde til sj -
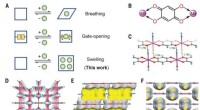 Brug af en manganpolymer til at adskille xylenisomererMn-dhbqs struktur og poreegenskaber. (A) Repræsentationer af forskellige former for rammedynamik eller fleksibilitet:vejrtrækning, portåbning-lukning eller linkerrotation og hævelse. (B) Koordinations
Brug af en manganpolymer til at adskille xylenisomererMn-dhbqs struktur og poreegenskaber. (A) Repræsentationer af forskellige former for rammedynamik eller fleksibilitet:vejrtrækning, portåbning-lukning eller linkerrotation og hævelse. (B) Koordinations
- SpaceX lancerer Air Forces bedste GPS hidtil, slutter bannerår
- Everglades viser forbedring i vandkvalitet
- Kitsch-religiøse souvenirs kan genoplive pilgrimsoplevelsen
- Hvad er formel for hastigheden af en bølge?
- Uddybende spørgsmål:Hvor godt forudsiger vi oversvømmelser?
- Materialer til den næste generation af elektronik og fotovoltaik


