Hvad er forholdet mellem reaktionens hastighed og hastigheden af dannelsen af produkter?
Der er en række faktorer, der kan påvirke hastigheden af en reaktion, herunder:
* Temperatur: Jo højere temperatur, jo hurtigere vil reaktionen ske. Dette skyldes, at højere temperaturer giver mere energi til reaktanterne, hvilket gør dem mere tilbøjelige til at kollidere og reagere.
* Koncentration: Jo højere koncentrationen af reaktanterne er, jo hurtigere vil reaktionen ske. Dette skyldes, at der er flere reaktanter tilgængelige til at kollidere med hinanden og reagere.
* Overfladeareal: Jo større overfladearealet af reaktanterne er, jo hurtigere vil reaktionen ske. Dette skyldes, at der er flere reaktanter tilgængelige til at kollidere med hinanden og reagere.
* Katalysatorer: Katalysatorer er stoffer, der fremskynder hastigheden af en reaktion uden at blive forbrugt i reaktionen. Katalysatorer virker ved at give en alternativ vej til reaktionen, som kræver mindre energi end den ukatalyserede reaktion.
Forholdet mellem hastigheden af en reaktion og hastigheden af produkter, der dannes, kan udtrykkes matematisk ved hjælp af følgende ligning:
```
rate =k[A]^n[B]^m
```
I denne ligning er hastigheden ændringen i produkternes koncentration over tid, k er hastighedskonstanten, [A] og [B] er koncentrationerne af reaktanterne, og n og m er rækkefølgen af reaktionen mhp. henholdsvis A og B.
Rækkefølgen af en reaktion er et mål for, hvordan reaktionshastigheden ændres med koncentrationen af reaktanterne. En førsteordensreaktion er en reaktion, hvor reaktionshastigheden er direkte proportional med koncentrationen af en af reaktanterne. En andenordensreaktion er en reaktion, hvor reaktionshastigheden er direkte proportional med koncentrationen af to af reaktanterne.
Hastighedskonstanten er en konstant, der afhænger af temperaturen og arten af reaktanterne. Hastighedskonstanten bruges til at beregne hastigheden af en reaktion ved en given temperatur og koncentration af reaktanterne.
Sidste artikelHvad er ethylelektronegativitet?
Næste artikelHvilken ladning er der på en ion med 35 protoner og 38 elektroner?
 Varme artikler
Varme artikler
-
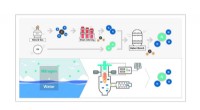 Den nye alkymi i kulstofneutralitet:At forvandle vand til ammoniak med kun vedvarende energi(Øverst) Harber-Bosch-metoden:brug af brint (ekstraheret ved termisk nedbrydning af naturgas) og atmosfærisk nitrogen som reaktanter, denne metode producerer ammoniak ved anvendelse af katalysator und
Den nye alkymi i kulstofneutralitet:At forvandle vand til ammoniak med kun vedvarende energi(Øverst) Harber-Bosch-metoden:brug af brint (ekstraheret ved termisk nedbrydning af naturgas) og atmosfærisk nitrogen som reaktanter, denne metode producerer ammoniak ved anvendelse af katalysator und -
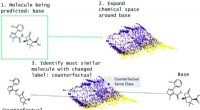 Brug af kontrafakta til at verificere forudsigelser om lægemiddelsikkerhedOversigt over MMACE. Inputtet er et molekyle, der skal forudsiges. Kemisk rum udvides og klynges. Kontrafakta er udvalgt fra klynger for at finde en kortfattet forklaring på forudsigelse af basemoleky
Brug af kontrafakta til at verificere forudsigelser om lægemiddelsikkerhedOversigt over MMACE. Inputtet er et molekyle, der skal forudsiges. Kemisk rum udvides og klynges. Kontrafakta er udvalgt fra klynger for at finde en kortfattet forklaring på forudsigelse af basemoleky -
 En brændstofkatalysator med højere udbytteKredit:Pixabay/CC0 Public Domain Oak Ridge National Laboratory-forskere har udviklet en ny katalysator til at omdanne ethanol til C3+ olefiner - de kemiske byggesten til vedvarende jetbrændstof og
En brændstofkatalysator med højere udbytteKredit:Pixabay/CC0 Public Domain Oak Ridge National Laboratory-forskere har udviklet en ny katalysator til at omdanne ethanol til C3+ olefiner - de kemiske byggesten til vedvarende jetbrændstof og -
 Nyt krystallinsk oxid kan løse problemet med overophedning i kompositmaterialerKredit:Toshihiro Isobe, Tokyo Institute of Technology Forskere ved Tokyo Institute of Technology har for nylig syntetiseret et nyt materiale, der viser unikke termiske ekspansionsegenskaber. Metod
Nyt krystallinsk oxid kan løse problemet med overophedning i kompositmaterialerKredit:Toshihiro Isobe, Tokyo Institute of Technology Forskere ved Tokyo Institute of Technology har for nylig syntetiseret et nyt materiale, der viser unikke termiske ekspansionsegenskaber. Metod
- Forskere udfører det første forbrændingseksperiment nogensinde med røntgenstråler
- Hvad betyder et vådt forår for skovbrandssæsonen?
- Afgrødeødelæggende armyorm-larver spredte sig til Uganda
- Undersøgelse finder et fald i stabiliteten af vandudbyttet i vandskel
- Forskere finder nanogaps i plasmoniske guldtråde øge spændingen, når de er spændte
- Et spor af galakser i hjertet af en gigantisk galaksehob


