Hvorfor ammoniak symmetrisk?
Symmetrien af ammoniak kan forstås ud fra molekylets molekylære orbitaler. Nitrogenatomet har fem valenselektroner, og disse elektroner optager tre sp3 hybridorbitaler. De tre sp3 hybridorbitaler er arrangeret i en tetraedrisk form, og de tre hydrogenatomer er bundet til nitrogenatomet gennem disse orbitaler.
Den fjerde valenselektron i nitrogenatomet optager en p-orbital. Denne p-orbital er vinkelret på planet af de tre sp3 hybridorbitaler, og den er ansvarlig for det enlige elektronpar på nitrogenatomet.
Symmetrien af ammoniak kan også forstås ud fra den molekylære punktgruppe. Ammoniakens punktgruppe er C3v, hvilket betyder, at molekylet har en tredobbelt rotationsakse, tre lodrette spejlplaner og et vandret spejlplan.
Ammoniakens symmetri har en række vigtige konsekvenser. For eksempel betyder symmetrien af molekylet, at de tre brintatomer alle er ækvivalente, og de har alle samme bindingslængde og bindingsvinkel. Molekylets symmetri betyder også, at molekylet har et dipolmoment, som er et mål for molekylets polaritet.
Sidste artikelHvordan finder man ud af et atoms kerneladning?
Næste artikelHvad er virkningerne af alkali?
 Varme artikler
Varme artikler
-
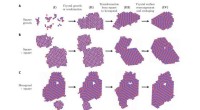 Team opdager, at polymorfe selektion under krystalvækst kan være termodynamisk drevetSnapshots fra MD-simuleringer af selvmontering med interaktionsstyrker EAA/EAB =EBB/EAB =0,15, temperatur kBT/EAB =0,1, og tæthed rs2 =0,1. Eksempler på kvadrat-til-hexagonale transformationer, der fo
Team opdager, at polymorfe selektion under krystalvækst kan være termodynamisk drevetSnapshots fra MD-simuleringer af selvmontering med interaktionsstyrker EAA/EAB =EBB/EAB =0,15, temperatur kBT/EAB =0,1, og tæthed rs2 =0,1. Eksempler på kvadrat-til-hexagonale transformationer, der fo -
 3D-print af stivelse til personlig udvikling af medicin3D-print gør det muligt at fremstille personaliserede lægemidler skræddersyet til den enkelte patient. Kredit:UPV/EHU Traditionelle metoder producerer lægemidler med specifikke parametre, men i man
3D-print af stivelse til personlig udvikling af medicin3D-print gør det muligt at fremstille personaliserede lægemidler skræddersyet til den enkelte patient. Kredit:UPV/EHU Traditionelle metoder producerer lægemidler med specifikke parametre, men i man -
 En grønnere vej til blå:Ny metode reducerer drastisk mængden af opløsningsmiddel, der er nødv…Udvikling af farvestofdannelse i løbet af 48 timers reaktionstid, efter opløsning af samme mængde faststof i samme mængde opløsningsmiddel. Kredit:Aalto University/Sandra Kaabel Phthalocyaniner bru
En grønnere vej til blå:Ny metode reducerer drastisk mængden af opløsningsmiddel, der er nødv…Udvikling af farvestofdannelse i løbet af 48 timers reaktionstid, efter opløsning af samme mængde faststof i samme mængde opløsningsmiddel. Kredit:Aalto University/Sandra Kaabel Phthalocyaniner bru -
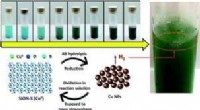 Forskere finder selvhelbredende katalysator til potentiel storstilet brug i brintproduktionForskerne overvejede regenerering, eller selvhelbredende -- katalysatorens evne til spontant at reparere sig selv under normale operationer -- er det mest attraktive træk. Kredit:EPFL Forskere, de
Forskere finder selvhelbredende katalysator til potentiel storstilet brug i brintproduktionForskerne overvejede regenerering, eller selvhelbredende -- katalysatorens evne til spontant at reparere sig selv under normale operationer -- er det mest attraktive træk. Kredit:EPFL Forskere, de
- Gendrivende teknologier til bevarelse af økosystemer:Brug med forsigtighed
- Nye ATLAS -præcisionsmålinger af Higgs Boson i den gyldne kanal
- Dramatiske vegetationsændringer i fortiden antyder en frygtelig fremtid
- Hvordan forskere kan bruge matematik fra det 19. århundrede til at bygge fremtidens computere
- Hvordan beskytter planter sig mod solskoldning?
- Telecomsendermaster kan bruges til at forudsige regn


