Hvad er pH-værdien af HCOOK?
En opløsnings pH defineres som den negative logaritme af hydrogenionkoncentrationen ([H+]). For en svag syre kan hydrogenionkoncentrationen beregnes ved hjælp af følgende ligning:
[H+] =Ka * [HCOK] / [KOG-]
hvor Ka er syredissociationskonstanten. Syredissociationskonstanten er et mål for styrken af en syre, og den er forskellig for hver syre.
For HCOOK er syredissociationskonstanten 1,8 x 10-4. Det betyder, at ved en koncentration på 1 M vil HCOOK dissociere til H+ og COOK-ioner i en udstrækning på 1,8 x 10-4 M.
pH-værdien af en 1 M opløsning af HCOOK kan beregnes ved hjælp af følgende ligning:
pH =-log[H+] =-log(1,8 x 10-4) =3,74
Derfor er pH-værdien af en 1 M opløsning af HCOOK 3,74.
Sidste artikelHvad er den gas, som mennesker skal indånde?
Næste artikelHvad udgør en atombombe?
 Varme artikler
Varme artikler
-
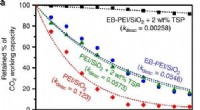 Forskere producerer 50x mere stabilt adsorbentKuldioxid arbejdskapacitet mod oxidativ ældningstid. Udførelsen af den foreslåede metode (sort) forringes meget langsommere (~ 50x) end eksisterende metoder. Det nye adsorbent er således vist at vær
Forskere producerer 50x mere stabilt adsorbentKuldioxid arbejdskapacitet mod oxidativ ældningstid. Udførelsen af den foreslåede metode (sort) forringes meget langsommere (~ 50x) end eksisterende metoder. Det nye adsorbent er således vist at vær -
 Forstå hvordan monomersekvens påvirker konduktans i molekylære ledningerForskere i Schroeder- og Moore-grupperne ved University of Illinois er interesserede i at bygge og studere kædemolekyler med høje præcisionsniveauer. På billedet fra venstre, Hao Yu, kandidatstuderend
Forstå hvordan monomersekvens påvirker konduktans i molekylære ledningerForskere i Schroeder- og Moore-grupperne ved University of Illinois er interesserede i at bygge og studere kædemolekyler med høje præcisionsniveauer. På billedet fra venstre, Hao Yu, kandidatstuderend -
 Forskerteam omvendt måde kaliumkanaler fungerer fra bakterier til menneskerGennem deres forskning, Cuello, sammen med D. Marien Cortes, bestemt, hvordan man får hidtil uset viden og kontrol over kaliumkanaler. Kredit:TTUHSC For første gang nogensinde, forskere ved Texas
Forskerteam omvendt måde kaliumkanaler fungerer fra bakterier til menneskerGennem deres forskning, Cuello, sammen med D. Marien Cortes, bestemt, hvordan man får hidtil uset viden og kontrol over kaliumkanaler. Kredit:TTUHSC For første gang nogensinde, forskere ved Texas -
 En lav pris, højeffektiv katalysator, der omdanner kuldioxid til andre kemikalierKatalysatoren udviklet af KISTs forskerhold bruger 20 % mindre iridium, et ædelmetal, end eksisterende katalysatorer og viser mindst 31 % højere ydeevne. En langtidstest med brug af postevand blev udf
En lav pris, højeffektiv katalysator, der omdanner kuldioxid til andre kemikalierKatalysatoren udviklet af KISTs forskerhold bruger 20 % mindre iridium, et ædelmetal, end eksisterende katalysatorer og viser mindst 31 % højere ydeevne. En langtidstest med brug af postevand blev udf
- Hvad er en X-bundet bærer homozygot?
- Cthulhu fossile rekonstruktion afslører monstrøse slægtninge til moderne havagurker
- Forskning peger på stærk indvirkning fra vandrensning til lægemiddelproduktion
- En lavtemperatur nanopartikelblæk
- En termisk isoleringskomposit af hule silicapartikler blandet med cellulosefibre
- Symbiotisk forhold mellem orkideen og træet


