Hvornår reagerer syrer med metaller?
- Saltdannelse:
Syrer reagerer med metaller og danner salte. Produktet af reaktionen er et salt og hydrogengas. For eksempel når saltsyre (HCl) reagerer med jern (Fe), dannes jern(II)chlorid (FeCl2) og brintgas (H2).
$$Fe_{(s)}+ 2HCl_{(aq)} \rightarrow FeCl_{2(aq)} + H_{2(g)}$$
- Frigivelse af brintgas:
Under reaktionen mellem syrer og metaller frigives brintgas. Dette skyldes, at syrer indeholder hydrogenioner (H+), som let reagerer med metallet og danner brintgas.
- Brusning:
Reaktionen mellem syrer og metaller frembringer ofte opbrusning, som er boblende eller brusende på grund af den hurtige frigivelse af brintgas. Den undslippende brintgas skaber bobler, der stiger op til væskens overflade.
- Varmeudvikling:
Reaktionen mellem syrer og metaller er normalt eksoterm, hvilket betyder, at den frigiver varme. Dette skyldes, at dannelsen af nye bindinger mellem metallet og ikke-metalionerne frigiver energi.
- Farveændring:
I nogle tilfælde kan reaktionen mellem syrer og metaller resultere i en farveændring. For eksempel, når kobber (Cu) reagerer med salpetersyre (HNO3), bliver opløsningen blå på grund af dannelsen af kobber(II)nitrat.
Samlet set involverer reaktionen mellem syrer og metaller dannelse af salt, frigivelse af brintgas, opbrusning, varmeudvikling og nogle gange farveændring.
Sidste artikelHvilke molekylære faststoffer har det højeste smeltepunkt?
Næste artikelHvorfor er natriumchlorid uopløseligt i ethylalkohol?
 Varme artikler
Varme artikler
-
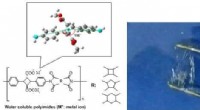 Højtermoresistente biopolyimider bliver vandopløselige som stivelseStrukturer af vandopløselige biopolyimider afledt af 4, 4-diaminotruxillinsyresalt med let bøjet struktur (model i toppen) og forskellige dianhydrider (venstre strukturer). Vandopløsende adfærd (højre
Højtermoresistente biopolyimider bliver vandopløselige som stivelseStrukturer af vandopløselige biopolyimider afledt af 4, 4-diaminotruxillinsyresalt med let bøjet struktur (model i toppen) og forskellige dianhydrider (venstre strukturer). Vandopløsende adfærd (højre -
 Genbrugte kontorstole omdannet til rygsække med hård skal og cykeltaskerKredit:Birmingham City University Gamle kontorstole omdannes til hårde rygsække og cykeltasker som en del af et innovativt nyt projekt. Thomas Howell-Jones, en produktdesignstuderende ved Birming
Genbrugte kontorstole omdannet til rygsække med hård skal og cykeltaskerKredit:Birmingham City University Gamle kontorstole omdannes til hårde rygsække og cykeltasker som en del af et innovativt nyt projekt. Thomas Howell-Jones, en produktdesignstuderende ved Birming -
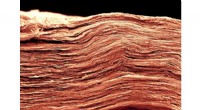 Højre elektrolyt fordobler nye todimensionelle materialers evne til at lagre energiI denne MXene elektrode, at vælge det passende opløsningsmiddel til elektrolytten kan øge energitætheden betydeligt. Dette scanningselektronmikroskopbillede viser fine træk af en film, der kun er 5 mi
Højre elektrolyt fordobler nye todimensionelle materialers evne til at lagre energiI denne MXene elektrode, at vælge det passende opløsningsmiddel til elektrolytten kan øge energitætheden betydeligt. Dette scanningselektronmikroskopbillede viser fine træk af en film, der kun er 5 mi -
 Undersøgelse af kemien i atomeksplosionerAerodynamisk begunstigede perfekt sfæriske jern- og aluminiumoxidkondensater blev genvundet ved hjælp af det nyligt udviklede eksperimentelle setup ved Lawrence Livermore National Laboratory. Uranoxid
Undersøgelse af kemien i atomeksplosionerAerodynamisk begunstigede perfekt sfæriske jern- og aluminiumoxidkondensater blev genvundet ved hjælp af det nyligt udviklede eksperimentelle setup ved Lawrence Livermore National Laboratory. Uranoxid
- Forskere skaber den første model for, hvordan plastikaffald bevæger sig i miljøet
- Forskere måler en-foton overgange i en ubundet elektron
- Her er, hvad vi ved om, hvordan klimaændringer giver næring til orkaner
- Hvor langt er jorden fra Venus?
- Hvad er pH i mælk?
- Tyfonen rammer Japan, nærmer sig katastroferamte regioner


