Hvilken reaktant giver det laveste udbytte ved at begrænse mængden af produkt?
 Varme artikler
Varme artikler
-
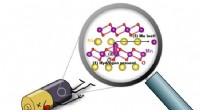 Mod et bedre batteri:Forskere afslører kilde til nedbrydning i natriumbatterierEn illustration viser hydrogen-induceret nedbrydning af et natrium-ion-batteri:(1) Når brint er til stede (cirklet med sort), (2) et Mn-atom (lilla) kan bevæge sig fra MnO2-laget til Na-laget (gult);
Mod et bedre batteri:Forskere afslører kilde til nedbrydning i natriumbatterierEn illustration viser hydrogen-induceret nedbrydning af et natrium-ion-batteri:(1) Når brint er til stede (cirklet med sort), (2) et Mn-atom (lilla) kan bevæge sig fra MnO2-laget til Na-laget (gult); -
 Kuldioxid-til-methanol-proces forbedret med katalysatorChunshan Song, venstre, og Xiao Jiang er to Penn State-forskere, der undersøger måder at bruge kuldioxid som råmateriale til at skabe brændstoffer og materialer. Song er direktør for EMS Energy Instit
Kuldioxid-til-methanol-proces forbedret med katalysatorChunshan Song, venstre, og Xiao Jiang er to Penn State-forskere, der undersøger måder at bruge kuldioxid som råmateriale til at skabe brændstoffer og materialer. Song er direktør for EMS Energy Instit -
 Superladede biomakromolekyler kan opretholde deres omordnede strukturer induceret, for eksempel, ved…Kredit:Wiley Stimuli-følsomme materialer kan reagere på fysiske kræfter med strukturelle faseovergange. Dette gælder også for blandinger af biopolymer og overfladeaktive stoffer, en undersøgelse f
Superladede biomakromolekyler kan opretholde deres omordnede strukturer induceret, for eksempel, ved…Kredit:Wiley Stimuli-følsomme materialer kan reagere på fysiske kræfter med strukturelle faseovergange. Dette gælder også for blandinger af biopolymer og overfladeaktive stoffer, en undersøgelse f -
 Nye materialer kunne drive sårheling ved at udnytte naturlige helingsmetoderKredit:CC0 Public Domain Materialer er meget brugt til at hjælpe med at hele sår:Kollagensvampe hjælper med at behandle forbrændinger og tryksår, og stilladslignende implantater bruges til at repa
Nye materialer kunne drive sårheling ved at udnytte naturlige helingsmetoderKredit:CC0 Public Domain Materialer er meget brugt til at hjælpe med at hele sår:Kollagensvampe hjælper med at behandle forbrændinger og tryksår, og stilladslignende implantater bruges til at repa
- Kulstofrige exoplaneter kan være lavet af diamanter
- Erfaringer fra det sydlige Australiens forretningsopsving midt i skovbrande og pandemi
- Hvad er standardtesten for ammoniakgas?
- Er teamvidenskab produktiv? Undersøgelse måler den kollaborative karakter af translationel medicin…
- Et overraskende stort sort hul kunne have slugt en stjerne indefra og ud, og videnskabsmænd er forv…
- Satellitgalakser ved udkanten af Mælkevejen sameksisterer med mørkt stof


