Hvor mange elektrondomæner er der omkring svovlen i SF4?
En trin-for-trin løsning:
Valenselektronkonfigurationen af svovl i dets elementære form er 3s23p4. Hvert fluoratom bidrager med en elektron til at danne en binding til svovl, hvilket resulterer i i alt 4 + 4 x 7 =32 elektroner i SF4. For at bestemme elektrondomænets geometri skal vi først beregne det steriske tal, som er summen af antallet af bundne atomer og ensomme par omkring et centralt atom. I SF4 er svovlatomet bundet til fire fluoratomer og har ét ensomt par, hvilket giver det et sterisk tal på 5. Dette svarer til en trigonal bipyramidal elektrondomæne-geometri.
Sidste artikelEr mikrobølger fysiske eller kemiske ændringer?
Næste artikelHvor mange elektroner har germanium?
 Varme artikler
Varme artikler
-
 Transparente belægninger til hverdagsbrugFluoroporbelægning på en tynd kobberfilm. Kredit:Bastian E. Rapp, SÆT Vand- og smudsafvisende sportstøj og udendørstøj, eller anti-dug forruder – der er mange hverdagsprodukter, der kan drage ford
Transparente belægninger til hverdagsbrugFluoroporbelægning på en tynd kobberfilm. Kredit:Bastian E. Rapp, SÆT Vand- og smudsafvisende sportstøj og udendørstøj, eller anti-dug forruder – der er mange hverdagsprodukter, der kan drage ford -
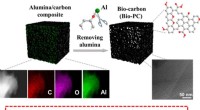 Grænseflade-induceret fremstilling af porøst kulstof med forbedrede iboende aktive stederUnder ikke-oxidationsbetingelser blev in-situ dannet aluminiumoxid/carbon-grænseflade udviklet som en vugge til generering af tilgængelige aktive steder. Det kan også justere den porøse struktur af re
Grænseflade-induceret fremstilling af porøst kulstof med forbedrede iboende aktive stederUnder ikke-oxidationsbetingelser blev in-situ dannet aluminiumoxid/carbon-grænseflade udviklet som en vugge til generering af tilgængelige aktive steder. Det kan også justere den porøse struktur af re -
 At møde en 100 år gammel udfordring kan føre vejen til digitale aromaerLugte kan måles ved deres afstand fra hinanden. Kredit:Weizmann Institute of Science Dufte – der lover mystik og intriger – blandes af mesterparfumører, deres opskrifter holdt hemmelige. I en ny u
At møde en 100 år gammel udfordring kan føre vejen til digitale aromaerLugte kan måles ved deres afstand fra hinanden. Kredit:Weizmann Institute of Science Dufte – der lover mystik og intriger – blandes af mesterparfumører, deres opskrifter holdt hemmelige. I en ny u -
 Forskere peger på, hvordan sorberende materialer fanger og frigiver kulstofKredit:Unsplash/CC0 Public Domain En nøglekomponent i DAC-systemer (ambient direct air capture), der fjerner kuldioxid fra luften, er det sorberende materiale, der bruges til først at opfange kuls
Forskere peger på, hvordan sorberende materialer fanger og frigiver kulstofKredit:Unsplash/CC0 Public Domain En nøglekomponent i DAC-systemer (ambient direct air capture), der fjerner kuldioxid fra luften, er det sorberende materiale, der bruges til først at opfange kuls
- Boeing Starliner-astronauter:Hvad seks måneder fast i rummet kan gøre ved deres opfattelse af tid
- Nye teknikker forbedrer kvantekommunikation, indvikle fononer
- En istid, der varer 115, 000 år på to minutter
- Var Beethoven sort? Et Twitter-meme afslører mere om race og musik end komponisterne opstår
- Hvad ville danne en elektrolytopløsning?
- Er transgen bomuld mere rentabelt?


