Bestem reaktionsvarmen for disse kemiske reaktioner. Er de endo- eller eksoterme 1. C s H 2 O g CO 2. Jeg kan tilsyneladende ikke få samme svar to gange. Kan nogen hjælpe mig?
>Forbrænding af metan:
```
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
```
Entalpiændring: AH =-890 kJ/mol
Denne reaktion er exoterm fordi det afgiver varme til omgivelserne.
---
2.
>Dekomponering af vand:
```
2H2O(l) → 2H2(g) + O2(g)
```
Entalpiændring: ΔH =+286 kJ/mol
Denne reaktion er endoterm fordi den optager varme fra omgivelserne.
 Varme artikler
Varme artikler
-
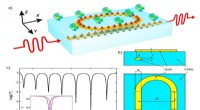 Blod og sved:Bærbare medicinske sensorer vil få et stort følsomhedsforøgelseBiosensor layout (en, c). Bølgelederen er inde i det dielektriske substrat. Resonatoren, realiseret som en ringbølgeleder, er placeret ved grænsefladen mellem det dielektriske materiale og den biologi
Blod og sved:Bærbare medicinske sensorer vil få et stort følsomhedsforøgelseBiosensor layout (en, c). Bølgelederen er inde i det dielektriske substrat. Resonatoren, realiseret som en ringbølgeleder, er placeret ved grænsefladen mellem det dielektriske materiale og den biologi -
 Astrokemi:hvordan livet kan være begyndt i rummetHvordan forskerne replikerer rumstråling i laboratoriet:en lyskilde stimulerer brint og skaber dermed energirig ultraviolet stråling. Kredit:RUB, Damian Gorczany Vi forestiller os normalt kometpåv
Astrokemi:hvordan livet kan være begyndt i rummetHvordan forskerne replikerer rumstråling i laboratoriet:en lyskilde stimulerer brint og skaber dermed energirig ultraviolet stråling. Kredit:RUB, Damian Gorczany Vi forestiller os normalt kometpåv -
 Et skridt hen imod syntese af metalorganiske strukturerKredit:Catalan Institute of Nanoscience and Nanotechnology Dr. Inhar Imaz og ICREA-professor Daniel Maspoch er hjernen bag en ny metode til organisk metalstruktursyntese. Deres spraytørringsteknik
Et skridt hen imod syntese af metalorganiske strukturerKredit:Catalan Institute of Nanoscience and Nanotechnology Dr. Inhar Imaz og ICREA-professor Daniel Maspoch er hjernen bag en ny metode til organisk metalstruktursyntese. Deres spraytørringsteknik -
 Ny metode til konstruktion af metaboliske vejeKredit:CC0 Public Domain Celler er utroligt dygtige til at skabe komplekse molekyler, ligesom terapi, og kan gøre så meget bedre end mange af vores bedste fabrikker. Syntetiske biologer søger at
Ny metode til konstruktion af metaboliske vejeKredit:CC0 Public Domain Celler er utroligt dygtige til at skabe komplekse molekyler, ligesom terapi, og kan gøre så meget bedre end mange af vores bedste fabrikker. Syntetiske biologer søger at
- De tørste steder på jorden med den mindste regn
- Hvordan man dyrer løvfugle
- Hvad er virkningen af frostvæske på miljøet?
- Hvordan kan Illinois løse problemet med PFAS-forurening?
- Hvordan fremstilles brintgas i laboratoriet?
- Forskere viser, at solens magnetiske aktivitet påvirker bestemmelsen af dens seismiske alder


