Hvordan kombineres atomer og danner molekyler gennem ionbinding?
1. Elektronoverførsel :
- Atomer involveret i ionbinding har forskellige elektronegativiteter, hvilket betyder, at deres evne til at tiltrække elektroner varierer.
- Atomet med højere elektronegativitet (højere tendens til at tiltrække elektroner) får elektroner fra atomet med lavere elektronegativitet.
2. Iondannelse :
- Som følge af elektronoverførsel mister det elektrondonerende atom elektroner og bliver positivt ladet og danner en kation (positivt ladet ion).
- Det elektronmodtagende atom optager elektroner og bliver negativt ladet og danner en anion (negativt ladet ion).
3. Elektrostatisk tiltrækning :
- De modsat ladede ioner bliver elektrostatisk tiltrukket af hinanden på grund af deres modsatte ladninger.
- Den elektrostatiske kraft mellem de positive og negative ioner holder dem sammen og danner en ionbinding.
4. Krystalgitterdannelse :
- I ionforbindelser er ionerne arrangeret i et regulært, gentagende mønster kaldet et krystalgitter.
- Ionerne pakker sig tæt sammen for at maksimere den elektrostatiske tiltrækning mellem dem, hvilket resulterer i en stabil ionforbindelse.
5. Støkiometri :
- Antallet af overførte elektroner og forholdet mellem positive og negative ioner i en ionforbindelse bestemmes af valenserne (antal valenselektroner) af de deltagende atomer.
- Dette forhold sikrer elektrisk neutralitet, hvor den samlede positive ladning af kationer er lig med den samlede negative ladning af anioner.
Eksempler på ionbinding omfatter natriumchlorid (NaCl), hvor natrium overfører en elektron til chlor og danner Na+ og Cl-ioner, der holdes sammen af ionbindinger. Tilsvarende mister calcium i calciumfluorid (CaF2) to elektroner til fluor og danner Ca2+ og 2F-ioner, der danner en ionisk forbindelse.
Ionbinding er almindeligvis observeret i forbindelser dannet mellem metaller og ikke-metaller. Styrken og stabiliteten af ionbindinger afhænger af ladningen af ionerne og størrelsesforskellen mellem ionerne.
Sidste artikelHvad er oxidationstallet for ZnHSO32?
Næste artikelHvad er sikre niveauer af svovlbrinte i klor svømmebassiner?
 Varme artikler
Varme artikler
-
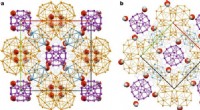 To Frank-Kasper faser i saltkrystalstrukturer observereten, Fase 1. b, Fase 2. Klynger A1, A2, B og C er farvet i lilla, orange, blå og grå, henholdsvis. I begge strukturer, lidelse er blevet fjernet for klarhedens skyld. Chlorider er blevet forbundet for
To Frank-Kasper faser i saltkrystalstrukturer observereten, Fase 1. b, Fase 2. Klynger A1, A2, B og C er farvet i lilla, orange, blå og grå, henholdsvis. I begge strukturer, lidelse er blevet fjernet for klarhedens skyld. Chlorider er blevet forbundet for -
 I betragtning af virkningen af den indendørs kemi -cocktailKredit:CC0 Public Domain Et par forskere, et med det kinesiske videnskabsakademi i Kina, den anden med University of Toronto i Canada har genbesøgt emnet indendørs kemi og dens indvirkning på menn
I betragtning af virkningen af den indendørs kemi -cocktailKredit:CC0 Public Domain Et par forskere, et med det kinesiske videnskabsakademi i Kina, den anden med University of Toronto i Canada har genbesøgt emnet indendørs kemi og dens indvirkning på menn -
 Hurtig test for at sikre høj mælkekvalitetChip med integreret lyskilde og lysdetektor til analyse af forurenende stoffer i mælk. Kredit:Fraunhofer-Gesellschaft Standarder for fødevaresikkerhed og fødevarekvalitet har aldrig været højere i
Hurtig test for at sikre høj mælkekvalitetChip med integreret lyskilde og lysdetektor til analyse af forurenende stoffer i mælk. Kredit:Fraunhofer-Gesellschaft Standarder for fødevaresikkerhed og fødevarekvalitet har aldrig været højere i -
 Tilføjelse af kobber styrker 3-D-printet titanium3D-printede titanium-kobber stænger med titanium pulver og kobber pulver. Kredit:RMIT University Vellykkede forsøg med titanium-kobber-legeringer til 3-D-print kan kickstarte en ny serie af højtyd
Tilføjelse af kobber styrker 3-D-printet titanium3D-printede titanium-kobber stænger med titanium pulver og kobber pulver. Kredit:RMIT University Vellykkede forsøg med titanium-kobber-legeringer til 3-D-print kan kickstarte en ny serie af højtyd
- Æble dingler flere lækkerier, mens du tilføjer tekniske diætmuligheder (Opdatering)
- Robotter kan ikke løbe fra dyr. En ny undersøgelse undersøger hvorfor
- Seks ting, Australien har brug for i sin nationale elbilstrategi
- Billede:Hubbles dværgstørrelse, dobbelt navngivet galakse
- Grundvandspumpning har reduceret amerikanske strømme betydeligt
- Tesla -aktionærer afviser bud om at fratage Musk formandsposten


