Hvilken masse skal der til for at få 2N opløsning af Na2co3 til at beregne sodimcarbonat, som vil blive opløst i 500 ccc?
Her vil vi lave en 2N-løsning. Så normalitet (N) =2
Givet volumen =500 ml =0,5 L
Formlen til at beregne antallet af krævede mol opløst stof er:
Antal mol =Normalitet × Opløsningens rumfang i liter
Beregn først antallet af nødvendige mol Na2CO3.
Antal mol =Normalitet × Opløsningsvolumen i liter
=2 N × 0,5 L
=1 mol
Vi skal opløse 1 mol Na2CO3 i 500 ml vand for at lave en 2N opløsning.
Beregn nu den nødvendige masse af Na2CO3.
Molær masse af Na2CO3 =106 g/mol (natrium:2 × 23 g/mol, kulstof:1 × 12 g/mol, oxygen:3 × 16 g/mol)
Masse =Antal mol × molær masse
Masse =1 mol × 106 g/mol
=106 gram
Derfor skal 106 gram Na2CO3 opløses i 500 ml vand for at lave en 2N opløsning.
Sidste artikelHvad bruges svovl til eller i?
Næste artikelHvordan forbereder du 0,05N HCl?
 Varme artikler
Varme artikler
-
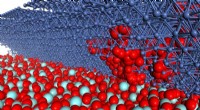 Atomisk præcise modeller forbedrer forståelsen af brændselscellerDe indledende positioner af atomerne i denne computermodel af en fast-oxid brændselscelle var baseret på observationer af den faktiske atomare konfiguration ved hjælp af elektronmikroskopi. Simulering
Atomisk præcise modeller forbedrer forståelsen af brændselscellerDe indledende positioner af atomerne i denne computermodel af en fast-oxid brændselscelle var baseret på observationer af den faktiske atomare konfiguration ved hjælp af elektronmikroskopi. Simulering -
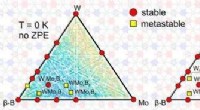 Forskere forudsiger nyt, hårdt, og superhårde ternære forbindelserTernær fasediagram over W-Mo-B-systemet ved 0 K. Kredit:A. Kvashnin et al./Chemistry of Materials Forskere fra Skolkovo Institute of Science and Technology (Skoltech), Institute of Solid State Che
Forskere forudsiger nyt, hårdt, og superhårde ternære forbindelserTernær fasediagram over W-Mo-B-systemet ved 0 K. Kredit:A. Kvashnin et al./Chemistry of Materials Forskere fra Skolkovo Institute of Science and Technology (Skoltech), Institute of Solid State Che -
 Bekæmpelse af lægemiddelresistens med hurtig, kunstig forstærkning af naturlige produkterForskere ved University of Tokyo bruger nye metoder til at imødegå den globale sundhedstrussel ved lægemiddelresistens og bygger nye antibiotika til at dræbe superbugen MRSA (methicillin-resistent Sta
Bekæmpelse af lægemiddelresistens med hurtig, kunstig forstærkning af naturlige produkterForskere ved University of Tokyo bruger nye metoder til at imødegå den globale sundhedstrussel ved lægemiddelresistens og bygger nye antibiotika til at dræbe superbugen MRSA (methicillin-resistent Sta -
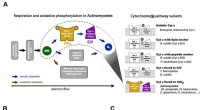 Klar til nærbilledet - en bakteries elektrontransportvejRespiration i Actinomycetes og overordnet arkitektur af Mycobacterial respiratorisk maskine CIII2CIV2SOD2. A) Den respiratoriske elektronoverførselskæde i Actinomycetes (venstre) og de 5 større prokar
Klar til nærbilledet - en bakteries elektrontransportvejRespiration i Actinomycetes og overordnet arkitektur af Mycobacterial respiratorisk maskine CIII2CIV2SOD2. A) Den respiratoriske elektronoverførselskæde i Actinomycetes (venstre) og de 5 større prokar
- US Interior Dept godkender olieboring i arktisk tilflugtssted
- Vugger menneskehedens vugge
- Kunne vi nogensinde udnytte kvantevakuumenergi?
- Lockdown ændrede irsk shopping- og madlavningsadfærd
- Mastercard forsøger at slette grænser for mindre virksomheder
- Forudsige effekten af klimaændringer på afgrødeudbyttet


