Hvorfor bruges en fast syre til at standardisere base?
Kaliumhydrogenphthalat bruges ikke som en primær standard for basestandardisering af flere årsager:
Svag surhedsgrad: KHP er en svag syre, hvilket betyder, at den delvist dissocierer i vand. Denne partielle dissociation resulterer i en lavere effektiv koncentration af hydrogenioner (H+) sammenlignet med stærke syrer som HCl. Usikkerheden forbundet med den partielle dissociation kan introducere fejl i standardiseringsprocessen.
Langsom reaktion: KHP reagerer relativt langsomt med baser. Denne langsomme reaktionshastighed kan føre til forlængede titreringstider og gøre det vanskeligt nøjagtigt at bestemme ækvivalenspunktet. Hurtigt reagerende syrer, som HCl, giver mere præcise og hurtige titreringsresultater.
Indvirkning af urenheder: KHP kan blive påvirket af urenheder og miljøforhold som f.eks. fugt. Absorbering af fugt fra luften kan ændre dens støkiometri og påvirke nøjagtigheden af standardiseringen. Stærke syrer som HCl er mindre modtagelige for sådanne påvirkninger og giver mere pålidelige resultater.
Derfor, mens KHP er en vigtig primær standard for syre-base titreringer, bruges den ikke almindeligvis til standardisering af baser på grund af dens svage surhedsgrad, langsomme reaktionshastighed og potentiale for urenheder. Stærke syrer som HCl foretrækkes generelt til dette formål på grund af deres høje surhedsgrad, hurtige reaktionskinetik og større pålidelighed.
 Varme artikler
Varme artikler
-
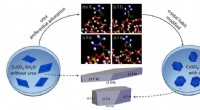 Virkningen af urinstofadditiver på krystallers fysisk -kemiske egenskaberSkematisk illustration af virkningen af urinstofadditiv på CuSO 4 · 5H 2 O krystalvane. Kredit:Prof. ZHUANGs gruppe) Krystalvaner har en betydelig indvirkning på krystallers fysisk -kemiske
Virkningen af urinstofadditiver på krystallers fysisk -kemiske egenskaberSkematisk illustration af virkningen af urinstofadditiv på CuSO 4 · 5H 2 O krystalvane. Kredit:Prof. ZHUANGs gruppe) Krystalvaner har en betydelig indvirkning på krystallers fysisk -kemiske -
 Forskere udvikler kryogen kaffekværnteknologiRegelmæssig (venstre) og kryogen (højre) slibning. Kredit:Coffeehouse Seneca Skoltech Ph.D. Dima Smirnov og hans kolleger fra St. Petersborg, Alexander Saichenko, Vladimir Dvortsov, Mikhail Tkache
Forskere udvikler kryogen kaffekværnteknologiRegelmæssig (venstre) og kryogen (højre) slibning. Kredit:Coffeehouse Seneca Skoltech Ph.D. Dima Smirnov og hans kolleger fra St. Petersborg, Alexander Saichenko, Vladimir Dvortsov, Mikhail Tkache -
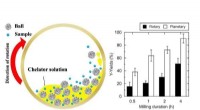 Forkortelse af sjældne jordarters forsyningskæde via genbrugFigur Skematisk afbildning af den chelator-assisteret våd-fræsning i en kuglemølle, og sammenligning af Y-udbyttet (procent) fra EoL-FL i roterende og planetariske kuglemøller. Kredit:Kanazawa Univers
Forkortelse af sjældne jordarters forsyningskæde via genbrugFigur Skematisk afbildning af den chelator-assisteret våd-fræsning i en kuglemølle, og sammenligning af Y-udbyttet (procent) fra EoL-FL i roterende og planetariske kuglemøller. Kredit:Kanazawa Univers -
 Forskere genskaber parfume fra det 17. århundrede af Constantijn HuygensEn krukke med ingredienserne til parfumen. Kredit:Leiden University Et team af forskere fra Young Academy og Huygens ING/NL Lab har bragt en tre århundreder gammel duft til live baseret på en opskr
Forskere genskaber parfume fra det 17. århundrede af Constantijn HuygensEn krukke med ingredienserne til parfumen. Kredit:Leiden University Et team af forskere fra Young Academy og Huygens ING/NL Lab har bragt en tre århundreder gammel duft til live baseret på en opskr


