Fryser alle væsker og gasser som vand?
Mens mange stoffer, herunder vand, gennemgår en faseovergang fra væske til fast ved afkøling, udviser nogle stoffer forskellig adfærd. Her er et par eksempler:
1. Helium:Helium er en gas ved stuetemperatur og atmosfærisk tryk. Det forbliver i en gasformig tilstand selv ved ekstremt lave temperaturer, såsom det absolutte nulpunkt (-273,15 grader Celsius eller -459,67 grader Fahrenheit). Heliums unikke egenskaber tilskrives dets ekstremt svage intermolekylære kræfter.
2. Ethanol (alkohol):Ethanol, almindeligvis kendt som ethylalkohol, har et frysepunkt på -114 grader Celsius (-173,2 grader Fahrenheit). I modsætning til vand, som danner iskrystaller ved frysning, størkner ethanol til et pulveragtigt stof kendt som "snekrystaller" eller "issne" på grund af dets forskellige molekylære struktur.
3. Kviksølv:Kviksølv er et metal, der er flydende ved stuetemperatur. Det har et frysepunkt på -38,83 grader Celsius (-37,89 grader Fahrenheit). Når det afkøles under dette punkt, bliver kviksølv et fast stof med et sølvhvidt udseende.
4. Kuldioxid:Kuldioxid er en gas ved stuetemperatur og -tryk. Det kan dog gøres flydende ved at påføre tryk eller afkøle det til under -78,5 grader Celsius (-110,3 grader Fahrenheit). Yderligere afkøling af flydende kuldioxid resulterer i dets størkning til "tøris", som sublimerer (transformeres direkte fra fast stof til gas) ved atmosfærisk tryk.
5. Nogle legeringer og polymerer:Visse legeringer og polymerer kan udvise glasovergangstemperaturer i stedet for særskilte frysepunkter. Disse materialer kan gradvist overgå fra en væskelignende tilstand til en fastlignende tilstand uden at danne en krystallinsk struktur.
Sammenfattende varierer stoffernes fryseadfærd afhængigt af deres kemiske og fysiske egenskaber. Mens mange væsker og gasser fryser ved afkøling, udviser nogle unikke frysepunkter eller danner forskellige faste strukturer.
Sidste artikelHvilken temperatur fryser gassen ved?
Næste artikelHvad er stærkere aluminium eller bobleplast?
 Varme artikler
Varme artikler
-
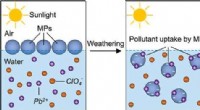 Forskere tager fat på miljøforvitring af mikroplast, optagelse af forurenende stofferGrafisk abstrakt. Kredit:ACS Environmental Au (2022). DOI:10.1021/acsenvironau.2c00036 I et nyt papir fra fakultet og studerende i LSU Chemical Engineering and Chemistry offentliggjort i ACS Enviro
Forskere tager fat på miljøforvitring af mikroplast, optagelse af forurenende stofferGrafisk abstrakt. Kredit:ACS Environmental Au (2022). DOI:10.1021/acsenvironau.2c00036 I et nyt papir fra fakultet og studerende i LSU Chemical Engineering and Chemistry offentliggjort i ACS Enviro -
 Forskere udvikler en ny membranløs brændselscelleKredit:Pixabay/CC0 Public Domain Forskerholdet af INRS professor Mohamed Mohamedi har designet en grøn membranløs brændselscelle, der bruger ilt fra luften. Resultaterne af denne innovative mikrof
Forskere udvikler en ny membranløs brændselscelleKredit:Pixabay/CC0 Public Domain Forskerholdet af INRS professor Mohamed Mohamedi har designet en grøn membranløs brændselscelle, der bruger ilt fra luften. Resultaterne af denne innovative mikrof -
 Ny teknologi identificerer konsekvent proteiner fra et dusin cellerSammensmeltning af mikrofluidik og robotteknologi, forskere har udviklet en ny prøveudtagningsplatform, der giver aldrig-før-mulig indsigt i proteiner hos mennesker, dyr, og planteceller. Kredit:US De
Ny teknologi identificerer konsekvent proteiner fra et dusin cellerSammensmeltning af mikrofluidik og robotteknologi, forskere har udviklet en ny prøveudtagningsplatform, der giver aldrig-før-mulig indsigt i proteiner hos mennesker, dyr, og planteceller. Kredit:US De -
 Siger mod at forbedre fælles forbindelsesteknologier til letvægts- og højstyrkestrukturerTynd GFRP forstærkning. Kredit:Toyohashi University of Technology. Forskerholdet (ledet af professor Yukihiro Matsumoto) dannet af Institut for Arkitektur og Bygningsteknik ved Toyohashi University
Siger mod at forbedre fælles forbindelsesteknologier til letvægts- og højstyrkestrukturerTynd GFRP forstærkning. Kredit:Toyohashi University of Technology. Forskerholdet (ledet af professor Yukihiro Matsumoto) dannet af Institut for Arkitektur og Bygningsteknik ved Toyohashi University
- Flerfarvede lette snoninger på nye knudrede måder
- Mus, der navigerer i et virtual reality-miljø, afslører, at vægge, ikke gulve, definerer rummet
- Undersøgelse finder en enkel forklaring på religionens udholdenhed
- Det er usandsynligt at nå det nationale mål for elbiler inden 2030 uden lavere priser, bedre polit…
- Hvad kaldes en beskrivelse af, hvor langt det er fra et punkt til et andet målt i samlet længde?
- På en campingvogn, med en af Saharas sidste europæiske opdagelsesrejsende


