Hvad sker der, når en væske afkøles til dets frysepunkt?
Når en væske fryser, frigiver den varmeenergi kendt som den latente fusionsvarme. Denne energi er nødvendig for at bryde de intermolekylære bindinger mellem de flydende molekyler og tillade dem at omarrangere til en fast struktur. Den latente fusionsvarme er specifik for hvert stof og er typisk en betydelig mængde energi.
Fryseprocessen kan forekomme gradvist eller hurtigt, afhængigt af flere faktorer, såsom afkølingshastigheden, tilstedeværelsen af urenheder og overfladearealet, der udsættes for det kolde miljø. Hurtig frysning resulterer i mindre iskrystaller, mens langsom frysning giver større krystaller. Urenheder kan fungere som kernedannelsessteder, fremme dannelsen af iskrystaller og fremskynde frysningsprocessen.
Frysning er en livsvigtig proces i naturen. Det spiller en afgørende rolle i vejr- og klimafænomener, herunder dannelsen af snefnug, hagl og iskapper. I hverdagen bruges frysning i køling og fødevarekonservering for at hæmme væksten af mikroorganismer og forlænge holdbarheden af letfordærvelige genstande.
 Varme artikler
Varme artikler
-
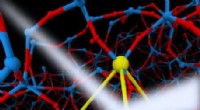 Hvad forårsager den top? Besvarelse af et langvarigt spørgsmål om kovalente væskerRøntgenspredning (hvid beem) billede af lokal tetraedrisk orden dannet af Si-atomer (store gule partikler) i flydende silica (Si-atomer er store partikler og O-atomer er små partikler) ved simulering.
Hvad forårsager den top? Besvarelse af et langvarigt spørgsmål om kovalente væskerRøntgenspredning (hvid beem) billede af lokal tetraedrisk orden dannet af Si-atomer (store gule partikler) i flydende silica (Si-atomer er store partikler og O-atomer er små partikler) ved simulering. -
 Kaffeforfalskning afdækket ved hjælp af ny metodeKredit:Quadram Institute Forskere fra Quadram Institute har udviklet en ny teknik til at skelne mellem overlegen Arabica -kaffe og billigere, lavere kvalitet Robusta. Ved hjælp af den nye teknik,
Kaffeforfalskning afdækket ved hjælp af ny metodeKredit:Quadram Institute Forskere fra Quadram Institute har udviklet en ny teknik til at skelne mellem overlegen Arabica -kaffe og billigere, lavere kvalitet Robusta. Ved hjælp af den nye teknik, -
 Biofornyelig proces kan hjælpe grøn plastKrystal af furandicarboxylsyre, eller FDCA, en plastikforløber skabt med biomasse i stedet for olie. Kredit:UW-Madison-billede af Ali Hussain Motagamwala og James Runde Da John Wesley Hyatt patent
Biofornyelig proces kan hjælpe grøn plastKrystal af furandicarboxylsyre, eller FDCA, en plastikforløber skabt med biomasse i stedet for olie. Kredit:UW-Madison-billede af Ali Hussain Motagamwala og James Runde Da John Wesley Hyatt patent -
 Team opdager dobbelt helixstruktur i syntetisk makromolekyleLou Madsen (tv.) er lektor i Kemisk Institut og har ledet et internationalt tværfagligt samarbejde om opdagelsen af den dobbelte helixstruktur af en polymer kaldet PBDT. Ying Wang (th.) er en tidlig
Team opdager dobbelt helixstruktur i syntetisk makromolekyleLou Madsen (tv.) er lektor i Kemisk Institut og har ledet et internationalt tværfagligt samarbejde om opdagelsen af den dobbelte helixstruktur af en polymer kaldet PBDT. Ying Wang (th.) er en tidlig
- Datadrevet beslutningsproces kan blive lettere i byggesektoren
- Hvor havet møder himlen, kemikere leder efter spor til vores klima
- Opdagelse af naturligt chirale overflader til sikrere lægemidler
- Hvem opfandt elevatoren?
- Resistive hukommelseskomponenter computerindustrien kan ikke modstå
- Kvantematerialers subtile spinadfærd beviser teoretiske forudsigelser


