Hvad er den empiriske formel for en forbindelse, der indeholder 57 vægtprocent svovl og 43 ilt?
For at beregne den empiriske formel antager vi, at vi har \(100\) g af forbindelsen. Derfor vil vi have:\(57\) g \(S\) og \(43\) g \(O\).
Beregn antallet af mol af \(S\):
$$57\ g\ S \time \frac{1\ mole\ S}{32\ g\ S} =1,78 \ mol \ S$$
Beregn antallet af mol af \(O\):
$$43\ g\ O \time \frac{1\ mol \ O}{16\ g\ O} =2,7 \ mol\ O$$
Vi dividerer antallet af mol af hvert grundstof med det mindste antal mol, som er \(1,78\) mol:
$$1,78 \ mol \ S /1,78 \ mol =1\ S$$
$$2,70 \ mol \ O /1,78 \ mol =1,521 \ ca. 3 \ O$$
Derfor er den empiriske formel \(SO_{3}\)
Sidste artikelHvor meget masse har 1 mol svovlatomer?
Næste artikelBlandes opløsninger af sølvnitrat og lithiumbromid?
 Varme artikler
Varme artikler
-
 Forskere opdager ny struktur for lovende materialeklasserBiwu Ma, professor i kemi og biokemi, offentliggjort en ny undersøgelse om, hvordan en ny struktur kunne skabe blåt lys i en type materiale kaldet en perovskit. Kredit:Florida State University Flo
Forskere opdager ny struktur for lovende materialeklasserBiwu Ma, professor i kemi og biokemi, offentliggjort en ny undersøgelse om, hvordan en ny struktur kunne skabe blåt lys i en type materiale kaldet en perovskit. Kredit:Florida State University Flo -
 Nanoteknologi gør det muligt for ingeniører at svejse tidligere usvejsbare aluminiumslegeringerTo stykker aluminiumslegering 7075 svejset sammen ved hjælp af en nanopartikel-forstærket fyldtråd. Kredit:Oszie Tarula/UCLA En aluminiumslegering udviklet i 1940erne har længe holdt et løfte til
Nanoteknologi gør det muligt for ingeniører at svejse tidligere usvejsbare aluminiumslegeringerTo stykker aluminiumslegering 7075 svejset sammen ved hjælp af en nanopartikel-forstærket fyldtråd. Kredit:Oszie Tarula/UCLA En aluminiumslegering udviklet i 1940erne har længe holdt et løfte til -
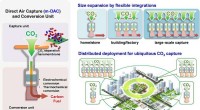 Membraner til at opfange kuldioxid fra luftenTeknologiske løsninger for CO2-emissionen til atmosfæren bør omfatte forskellige tilgange, da der ikke findes én silver bullet-løsning. I dette arbejde, forskere fra I2CNER, Kyushu University og NanoM
Membraner til at opfange kuldioxid fra luftenTeknologiske løsninger for CO2-emissionen til atmosfæren bør omfatte forskellige tilgange, da der ikke findes én silver bullet-løsning. I dette arbejde, forskere fra I2CNER, Kyushu University og NanoM -
 Nye beviser viser, at de første byggesten i livet på Jorden kan have været mere rodet end tidlige…Szostak mener, at de tidligste celler er udviklet på land i damme eller bassiner, potentielt i vulkansk aktive regioner. Ultraviolet lys, lynnedslag, og vulkanudbrud kunne alle have været med til at u
Nye beviser viser, at de første byggesten i livet på Jorden kan have været mere rodet end tidlige…Szostak mener, at de tidligste celler er udviklet på land i damme eller bassiner, potentielt i vulkansk aktive regioner. Ultraviolet lys, lynnedslag, og vulkanudbrud kunne alle have været med til at u
- Forskere løfter sløret for en ny teknik til forudsigelse af vulkanudbrud
- Hvor kommer den energi, der er nødvendig for stofskiftet, fra?
- Nyt værktøj til at måle aerosol optisk hygroskopicitet
- Kurdisk flygtning vinder Nobel of Mathematics Fields-medalje (opdatering)
- Hærens videnskabsmand studerer tordenvejr for at forbedre slagmarksmissioner
- Jeg kan ikke se race og andre hvide løgne


