Hvad er jernets atomare struktur?
Atomnummer: 26
Protoner: 26 protoner er placeret i kernen af et jernatom. Antallet af protoner i kernen definerer atomnummeret og bestemmer grundstoffets identitet.
Neutroner: Jernatomer har normalt 30 neutroner i kernen, men andre isotoper af jern kan have varierende antal neutroner. Neutroner bidrager til atomets samlede masse, men bærer ikke en elektrisk ladning.
Elektroner: Jern har 26 elektroner, der kredser om kernen i specifikke energiniveauer eller skaller. Disse elektroner er arrangeret i skaller baseret på deres energiniveauer.
Elektronkonfigurationen af jern er:
- K-skal:2 elektroner
- L skal:8 elektroner
- M-skal:14 elektroner
- N skal:2 elektroner
Valenselektroner: Den yderste skal af et atom, kendt som valensskallen, spiller en afgørende rolle i kemisk binding. I jern er valensskallen N-skallen, som har 2 elektroner. Disse valenselektroner er ansvarlige for at deltage i kemiske reaktioner og danne bindinger med andre atomer.
Den elektroniske konfiguration af jern kan repræsenteres som [Ar]3d64s2, hvilket indikerer tilstedeværelsen af seks elektroner i 3d subshell og to elektroner i 4s subshell.
Atomorbitaler: Elektronerne i de forskellige skaller optager atomare orbitaler, som er områder omkring kernen, hvor elektroner sandsynligvis vil blive fundet. 3d orbitaler spiller en væsentlig rolle i bestemmelsen af jerns magnetiske egenskaber og kemiske opførsel.
Jerns atomare struktur er ansvarlig for dets forskellige egenskaber, herunder dets styrke, holdbarhed, magnetiske modtagelighed og evne til at danne legeringer med andre metaller. Jern er et vigtigt element i mange industrier og har været afgørende for at forme den menneskelige civilisations teknologiske fremskridt gennem historien.
 Varme artikler
Varme artikler
-
 En hurtig, effektiv COVID-19-biosensor er under udviklingRajesh Sardar, center, taler med Omolade Olofintuyi, venstre, en bachelor fra Howard University, som forskede i en avanceret biosensor for COVID-19 i sit laboratorium denne sommer gennem et NSF-finans
En hurtig, effektiv COVID-19-biosensor er under udviklingRajesh Sardar, center, taler med Omolade Olofintuyi, venstre, en bachelor fra Howard University, som forskede i en avanceret biosensor for COVID-19 i sit laboratorium denne sommer gennem et NSF-finans -
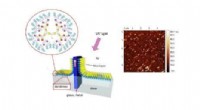 Forskere foreslår nyt materiale til ændring af overfladeegenskaberKredit:Skolkovo Institute of Science and Technology Forskere fra Skoltech Center for Design, Manufacturing and Materials (CDMM) foreslået at bruge sulfonimidbaserede dendrimerer til at lave tykfil
Forskere foreslår nyt materiale til ændring af overfladeegenskaberKredit:Skolkovo Institute of Science and Technology Forskere fra Skoltech Center for Design, Manufacturing and Materials (CDMM) foreslået at bruge sulfonimidbaserede dendrimerer til at lave tykfil -
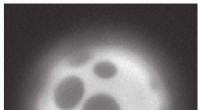 Levende cellemembraner kan selvsortere deres komponenter ved afblandingFaseadskillelse i en syntetisk membran. Kredit:Caitlin Cornell/University of Washington Celler - byggestenene i vores kroppe - er indkapslet af membraner. Det samme gælder de specialiserede rum i
Levende cellemembraner kan selvsortere deres komponenter ved afblandingFaseadskillelse i en syntetisk membran. Kredit:Caitlin Cornell/University of Washington Celler - byggestenene i vores kroppe - er indkapslet af membraner. Det samme gælder de specialiserede rum i -
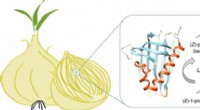 Den nitty-gritty bag hvordan løg får dig til at grædeKredit:American Chemical Society Tilføjelse af løg til en opskrift kan få et måltid til at smage rig og velsmagende, men at skære løget kan være brutalt. Løg frigiver en forbindelse kaldet lachrym
Den nitty-gritty bag hvordan løg får dig til at grædeKredit:American Chemical Society Tilføjelse af løg til en opskrift kan få et måltid til at smage rig og velsmagende, men at skære løget kan være brutalt. Løg frigiver en forbindelse kaldet lachrym
- Mens solvinden blæser, vores heliosfæreballoner
- Permafrost i Arktis kan tø hurtigere op end antaget
- #MeToo -stigning kan ændre samfundet på afgørende måder, siger analytikere
- Stedbaserede skatteincitamenter stimulerer beskæftigelsen i fjerntliggende regioner
- En magnetisk nanografen sommerfugl klar til at fremme kvanteteknologier
- Hvad er den mindste planet? (Det er ikke Pluto.) Ser nærmere på planetstørrelser.


