Hvor mange mol bariumnitrat BaNO3 indeholder 6,80X10 til de 24 formelenheder?
Trin 1:Konverter formelenheder til mol
Vi kan opsætte en konverteringsfaktor ved hjælp af Avogadros tal:
$$1 \text{ mol BaNO}_3 =6,022 \times 10^{23} \text{ formelenheder BaNO}_3$$
Ved at bruge denne omregningsfaktor kan vi konvertere det givne antal formelenheder til mol:
$$6,80 \times 10^{24} \text{ formelenheder BaNO}_3 \times \frac{1 \text{ mol BaNO}_3}{6,022 \times 10^{23} \text{ formelenheder BaNO}_3} =\boxed{11.31 \text{ mol BaNO}_3}$$
Derfor svarer 6,80 x 10^24 formelenheder af bariumnitrat til 11,31 mol BaNO3.
Sidste artikelHvor mange mol ammoniakgas findes der i en 202 ml beholder ved 35C og 750 mmHg?
Næste artikelHvad neutraliserer sur jord?
 Varme artikler
Varme artikler
-
 Lysemitterende elektrokemiske celler til genanvendelig belysningKredit:Technical University München En lavpris og let at fremstille lysteknologi kan fremstilles med lys-emitterende elektrokemiske celler. Sådanne celler er tyndfilm elektroniske og ioniske enhede
Lysemitterende elektrokemiske celler til genanvendelig belysningKredit:Technical University München En lavpris og let at fremstille lysteknologi kan fremstilles med lys-emitterende elektrokemiske celler. Sådanne celler er tyndfilm elektroniske og ioniske enhede -
 En bedre HIV-testCheng-ting Jason Tsai, en kandidatstuderende i laboratoriet hos Carolyn Bertozzi, og Peter Robinson, en tidligere kandidatstuderende hos Bertozzi, i 2016, arbejde på en tidligere version af deres test
En bedre HIV-testCheng-ting Jason Tsai, en kandidatstuderende i laboratoriet hos Carolyn Bertozzi, og Peter Robinson, en tidligere kandidatstuderende hos Bertozzi, i 2016, arbejde på en tidligere version af deres test -
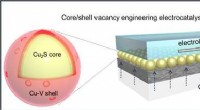 Ny katalysator opgraderer kuldioxid til fundne brændstofferCore/shell-vacancy engineering (CSVE) katalysator muliggør effektiv elektrokemisk reduktion af CO 2 til multi-carbon alkoholer. Kredit:ZHUANG Taotao Flydende multi-carbon alkoholer såsom ethanol
Ny katalysator opgraderer kuldioxid til fundne brændstofferCore/shell-vacancy engineering (CSVE) katalysator muliggør effektiv elektrokemisk reduktion af CO 2 til multi-carbon alkoholer. Kredit:ZHUANG Taotao Flydende multi-carbon alkoholer såsom ethanol -
 De miljømæssige omkostninger ved kontaktlinserKontaktlinser genvundet fra behandlet spildevandsslam kan skade miljøet. Kredit:Charles Rolsky Mange mennesker er afhængige af kontaktlinser for at forbedre deres syn. Men disse synskorrigerende e
De miljømæssige omkostninger ved kontaktlinserKontaktlinser genvundet fra behandlet spildevandsslam kan skade miljøet. Kredit:Charles Rolsky Mange mennesker er afhængige af kontaktlinser for at forbedre deres syn. Men disse synskorrigerende e
- Udvikling af en superbase-sammenlignelig oxynitrid-katalysator
- Hvorfor March Madness er en særlig tid på året for statsbudgetterne
- Bevæger Jorden sig rundt om solen i sin bane?
- Forskere kappes for at skabe mere modstandsdygtige koraller for at overleve i opvarmende have
- Teleskopvisning blev suspenderet, da demonstranter blokerer Hawaii-vejen
- År med ekstremer for skrumpende schweiziske gletsjere i 2018:undersøgelse


