Hvilken type binding er der i cadmiumsulfid?
Ionisk binding:
I CdS har cadmium (Cd) tendens til at miste to valenselektroner, hvilket resulterer i en positiv ladning på 2+ (Cd²⁺). Samtidig har svovl (S) en tendens til at vinde to elektroner, hvilket får en negativ ladning på 2- (S²⁻). Den elektrostatiske tiltrækning mellem disse modsat ladede ioner (Cd²⁺ og S²⁻) giver anledning til ionbinding.
Kovalent karakter:
Mens CdS primært er ionisk, udviser det også en vis grad af kovalent karakter. Denne kovalente karakter opstår på grund af overlapningen af elektronorbitaler mellem Cd- og S-atomerne. De fyldte 4d orbitaler af Cd kan interagere med de ledige 3p orbitaler af S, hvilket fører til dannelsen af kovalente bindinger.
Polarisering:
Den ioniske binding i CdS er yderligere påvirket af polarisering. På grund af forskellen i elektronegativitet mellem Cd og S (Cd:1,69, S:2,58), er elektronskyen let forvrænget mod det mere elektronegative svovlatom. Dette resulterer i en delvis positiv ladning på Cd og en delvis negativ ladning på S, hvilket indfører en vis grad af polaritet.
Samlet set udviser cadmiumsulfid ionbinding med en delvis kovalent karakter på grund af orbital overlapning og polarisationseffekter mellem Cd- og S-atomerne. Denne kombination af ionisk og kovalent binding bidrager til egenskaberne og karakteristika af CdS, såsom dets halvlederadfærd og fotokonduktivitet.
Sidste artikelEr massen af alle kloratomer altid 35,47?
Næste artikelOpløses brintoverilte i vand?
 Varme artikler
Varme artikler
-
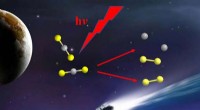 Dalian Coherent Light Source afslører oprindelsen af interstellar disulfurForskere observerede direkte C + S2-kanalen i CS 2 fotodissociation. Kredit:LI Zhenxing At studere skabelsen og udviklingen af svovlholdige forbindelser i det ydre rum er afgørende for at fors
Dalian Coherent Light Source afslører oprindelsen af interstellar disulfurForskere observerede direkte C + S2-kanalen i CS 2 fotodissociation. Kredit:LI Zhenxing At studere skabelsen og udviklingen af svovlholdige forbindelser i det ydre rum er afgørende for at fors -
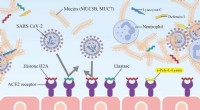 Ny nøglebeskyttelse mod COVID-19 fundet i spytSARS-CoV-2 overføres ved binding af spike-proteinet S1 på den virale kappe til den angiotensin-konverterende enzym 2 (ACE2)-receptor på plasmamembranen af humane celler. Histon H2A og elastaseprotei
Ny nøglebeskyttelse mod COVID-19 fundet i spytSARS-CoV-2 overføres ved binding af spike-proteinet S1 på den virale kappe til den angiotensin-konverterende enzym 2 (ACE2)-receptor på plasmamembranen af humane celler. Histon H2A og elastaseprotei -
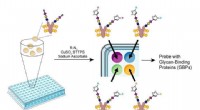 Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane
Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane -
 AI-agent hjælper med at identificere materialeegenskaber hurtigereKredit:CC0 Public Domain Effektiv analyse af røntgendiffraktionsdata (XRD) spiller en afgørende rolle i opdagelsen af nye materialer, for eksempel for fremtidens energisystemer. Det bruges til a
AI-agent hjælper med at identificere materialeegenskaber hurtigereKredit:CC0 Public Domain Effektiv analyse af røntgendiffraktionsdata (XRD) spiller en afgørende rolle i opdagelsen af nye materialer, for eksempel for fremtidens energisystemer. Det bruges til a
- Nanovidenskabens gennembrud:Undersøgelse af partikler mindre end en milliardtedel meter
- Forskere sikrer højopløsningsmålinger for CO2-diplomati
- Lukker Elon Musk en besværlig Twitter-konto eller driller den? (Opdatering)
- Sådan kontrolleres retningen af en Diode
- Hvordan man lærer en stjernes sande alder
- NASAs TESS-mission finder planeter med manglende led


