Når atommasserne af grundstoffer på det periodiske system stiger, hvad sker der med hvert antal atomer i 1 mol element?
For eksempel indeholder 1 mol brint 6,022 x 10^23 atomer, mens 1 mol bly kun indeholder 2,072 x 10^23 atomer. Dette skyldes, at bly har en meget højere atommasse end brint (207,2 amu vs. 1,008 amu), så der er færre blyatomer i 1 mol bly, end der er brintatomer i 1 mol brint.
Forholdet mellem atommasse og antallet af atomer i 1 mol af et grundstof er et vigtigt begreb i kemi, da det giver kemikere mulighed for at beregne massen af et givet antal atomer eller antallet af atomer i en given masse af et grundstof.
 Varme artikler
Varme artikler
-
 Højteknologisk sensing belyser betonstresstestEt billede fra et fotonisk kamera, der viser, hvordan brug af belægningen kan skabe en stearinlyslignende flamme, der fremhæver forskydningsspændingsfordelingen i en prøvebetonbjælke. Kredit:Universit
Højteknologisk sensing belyser betonstresstestEt billede fra et fotonisk kamera, der viser, hvordan brug af belægningen kan skabe en stearinlyslignende flamme, der fremhæver forskydningsspændingsfordelingen i en prøvebetonbjælke. Kredit:Universit -
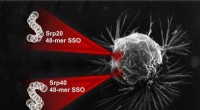 Biokemikere rapporterer en måde at stoppe kræftcellernes udødelighed med oligonukleotiderKredit:Natalia Deryugina RUDN biokemikere fandt en måde at reducere aktiviteten af telomerase (enzymet udødelighed af celler) 10 gange. Opdagelsen kan føre til nye antitumorlægemidler og give en
Biokemikere rapporterer en måde at stoppe kræftcellernes udødelighed med oligonukleotiderKredit:Natalia Deryugina RUDN biokemikere fandt en måde at reducere aktiviteten af telomerase (enzymet udødelighed af celler) 10 gange. Opdagelsen kan føre til nye antitumorlægemidler og give en -
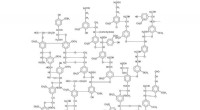 Dominerende svamp kunne være løsningen til at producere flere biobrændstoffer og kemikalierEt eksempel på en mulig ligninstruktur. Kredit:GFDL ver. 1.2 eller CC-by-sa ver. 2,5, 2.0, og 1.0 lub Public Domain (PD) Opdagelsen af et nyt enzym, der frigiver et værdifuldt kemikalie fra land
Dominerende svamp kunne være løsningen til at producere flere biobrændstoffer og kemikalierEt eksempel på en mulig ligninstruktur. Kredit:GFDL ver. 1.2 eller CC-by-sa ver. 2,5, 2.0, og 1.0 lub Public Domain (PD) Opdagelsen af et nyt enzym, der frigiver et værdifuldt kemikalie fra land -
 Video:Mærkelige ideer til at bekæmpe klimaændringerKredit:The American Chemical Society Der er ting, du kan gøre lige nu for at hjælpe vores klima – som at investere i vedvarende energi. Men i dag om reaktioner, vi graver i et par af de mærkeligs
Video:Mærkelige ideer til at bekæmpe klimaændringerKredit:The American Chemical Society Der er ting, du kan gøre lige nu for at hjælpe vores klima – som at investere i vedvarende energi. Men i dag om reaktioner, vi graver i et par af de mærkeligs
- NASA Armstrong opdaterer 1960'ernes koncept for at studere gigantiske planeter
- Hvad er de første eksperimenter i akustik blev udført af filosof og videnskabsmand?
- Video:Er der en hurtig løsning til havforsuring?
- Forskere opdager en ny måde at drive elektriske enheder på
- Forhindrer mere, henter mindre. Udbredelse af plastikforurening ændrer tilgang
- På duften af en førhistorisk partikelaccelerator?


