Hvilke produkter ville du få, når du bobler klorgas gennem en natriumbromidopløsning?
1. Danning af natriumchlorid (NaCl) :
Klorgas reagerer med bromidionerne (Br-) i natriumbromidopløsningen, hvilket resulterer i dannelsen af natriumchlorid (NaCl). Dette skyldes, at klor har en højere elektronegativitet end brom, så det har en tendens til at tiltrække elektroner fra bromidionerne og danner en kovalent binding med natriumioner (Na+).
2. Udgivelse af brom (Br2) :
Da klorgas reagerer med bromidioner, oxiderer den dem til dannelse af brommolekyler (Br2). Brom er et rødbrunt, flygtigt grundstof, der er mindre opløseligt i vand sammenlignet med klorgas. Derfor har den en tendens til at undslippe opløsningen som en gas.
Den samlede reaktion kan repræsenteres som følger:
```
Cl2(g) + 2NaBr(aq) → 2NaCl(aq) + Br2(g)
```
Sammenfattende, når klorgas bobles gennem en natriumbromidopløsning, resulterer det i dannelsen af natriumchlorid og frigivelsen af bromgas.
 Varme artikler
Varme artikler
-
 Forskere finder billigere, mindre energikrævende måde at rense ethylen påRasika Dias, UTA fremtrædende universitetsprofessor i kemi og biokemi Kredit:UTA Forskere ved University of Texas i Arlington har indgivet en foreløbig patentansøgning på en ny kobberforbindelse,
Forskere finder billigere, mindre energikrævende måde at rense ethylen påRasika Dias, UTA fremtrædende universitetsprofessor i kemi og biokemi Kredit:UTA Forskere ved University of Texas i Arlington har indgivet en foreløbig patentansøgning på en ny kobberforbindelse, -
 Atombilleder afslører mange naboer for nogle iltatomerBilleder af ilt (øverste række) og nitrogenatomer (nederste række) i et kulstofnetværk, optaget på mikroskopilaboratoriet ved universitetet i Wien. Blandt de forventede konfigurationer, ilt findes ogs
Atombilleder afslører mange naboer for nogle iltatomerBilleder af ilt (øverste række) og nitrogenatomer (nederste række) i et kulstofnetværk, optaget på mikroskopilaboratoriet ved universitetet i Wien. Blandt de forventede konfigurationer, ilt findes ogs -
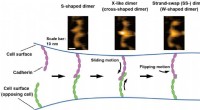 Visualisering af bindingsprocesser af celle-celle-adhæsionsmolekyler i opløsningHS-AFM billeder af cadherin dimererne er vist øverst. Bindingsmekanismen for cadheriner er illustreret i bunden baseret på HS-AFM-observationer. Kredit:Shigetaka Nishiguchi fra videnskabsmænd ved Expl
Visualisering af bindingsprocesser af celle-celle-adhæsionsmolekyler i opløsningHS-AFM billeder af cadherin dimererne er vist øverst. Bindingsmekanismen for cadheriner er illustreret i bunden baseret på HS-AFM-observationer. Kredit:Shigetaka Nishiguchi fra videnskabsmænd ved Expl -
 Dårligt guld kan trods alt være værdifuldtDette billede viser et eksempel på en krystal af jernsulfid dyrket i University of Minnesota lab til ekstrem høj renhed ved hjælp af en metode kaldet kemisk damptransport. Bemærk den gyldne glans, som
Dårligt guld kan trods alt være værdifuldtDette billede viser et eksempel på en krystal af jernsulfid dyrket i University of Minnesota lab til ekstrem høj renhed ved hjælp af en metode kaldet kemisk damptransport. Bemærk den gyldne glans, som
- Store områder i den brasilianske regnskov risikerer at miste beskyttelse
- Hvad er en B-celle?
- PPPL-forskere leverer ny højopløsningsdiagnostik til national laserfacilitet
- Nye beviser viser, at nuværende politikker ikke virker for at stoppe plastikforurening
- Hvad er en tankmotor,
- Undersøgelse beskriver tilstedeværelsen af tekstilmikrofibre i sydeuropæiske marinegulve


