Er bindingen mellem magnesium og ilt en ionisk eller aggregalent?
* Elektronegativitetsforskel: Magnesium (Mg) har en elektronegativitet på 1,31, mens ilt (O) har en elektronegativitet på 3,44. Forskellen i elektronegativitet er betydelig (2.13), hvilket indikerer en stærk tendens til, at ilt tiltrækker elektroner.
* Elektronoverførsel: Magnesium mister let sine to valenselektroner for at opnå en stabil oktet. Oxygen vinder på den anden side disse to elektroner til at afslutte sin oktet. Denne elektronoverførsel danner positivt ladede magnesiumioner (mg²⁺) og negativt ladede oxidioner (O²⁻).
* Elektrostatisk attraktion: De modsatte ladninger af ionerne tiltrækker hinanden og danner en elektrostatisk binding kendt som en ionisk binding.
Derfor er bindingen mellem magnesium og ilt i magnesiumoxid (MGO) primært ionisk.
 Varme artikler
Varme artikler
-
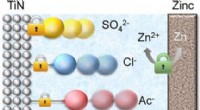 Zink-ion-hybridkondensatorer med ideelle anioner i elektrolytten viser ekstra lang ydelseKredit:Wiley Metal-ion hybrid kondensatorer kombinerer egenskaberne af kondensatorer og batterier. En elektrode bruger den kapacitive mekanisme, den anden redox-processer af batteritype. Forskere
Zink-ion-hybridkondensatorer med ideelle anioner i elektrolytten viser ekstra lang ydelseKredit:Wiley Metal-ion hybrid kondensatorer kombinerer egenskaberne af kondensatorer og batterier. En elektrode bruger den kapacitive mekanisme, den anden redox-processer af batteritype. Forskere -
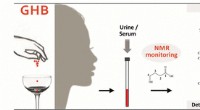 Forbedring af påvisning af et date-voldtægtsmiddelKredit:American Chemical Society Fordi gamma-hydroxysmørsyre (GHB), almindeligvis kendt som et dato-voldtægtsmiddel absorberes hurtigt og metaboliseres af kroppen, det er svært for ordensmagten at
Forbedring af påvisning af et date-voldtægtsmiddelKredit:American Chemical Society Fordi gamma-hydroxysmørsyre (GHB), almindeligvis kendt som et dato-voldtægtsmiddel absorberes hurtigt og metaboliseres af kroppen, det er svært for ordensmagten at -
 Laserskrivning kan muliggøre elektronisk næse til multigassensorAlexander Castonguay (til venstre), kandidatstuderende i laboratoriet for adjunkt Lauren Zarzar, og adjunkt Huanyu Larry Cheng brugte denne laseropsætning til deres tværfaglige samarbejde. Kredit:Kelb
Laserskrivning kan muliggøre elektronisk næse til multigassensorAlexander Castonguay (til venstre), kandidatstuderende i laboratoriet for adjunkt Lauren Zarzar, og adjunkt Huanyu Larry Cheng brugte denne laseropsætning til deres tværfaglige samarbejde. Kredit:Kelb -
 Opdagelse af, hvordan mennesker oplever lugten af død, kan redde livEdvard Munchs Lugten af død. Og himlen så på det fantastiske kadaver Blomstrer som en blomst. Så forfærdelig var stanken, at du troede Du ville besvime på græsset. Slagfluerne summede rundt
Opdagelse af, hvordan mennesker oplever lugten af død, kan redde livEdvard Munchs Lugten af død. Og himlen så på det fantastiske kadaver Blomstrer som en blomst. Så forfærdelig var stanken, at du troede Du ville besvime på græsset. Slagfluerne summede rundt
- Eksperimentel haveundersøgelse bruger AI til at vise, hvordan planter reagerer på miljøændringer…
- Hvilken bølgeegenskab stiger, når antallet af frembringende vibrationer stiger?
- Gamle enzymer katalysatorer for nye opdagelser
- Hvad er i horisonten for globale kulstofemissioner?
- Hvad er bulkdensitet?
- Eksperter udvikler nanolasere på silicium


