Hvordan adskiller de to isotoper af arsen fra hinanden?
* Antal neutroner: Dette er den vigtigste forskel.
* ⁷⁵as har 42 neutroner (75 - 33 =42).
* ⁷⁴as har 41 neutroner (74 - 33 =41).
* atommasse: Mens antallet af protoner (33) er det samme for begge isotoper, resulterer det forskellige antal neutroner i en lidt anden atommasse.
* ⁷⁵as har en atommasse på cirka 74.9225 amu.
* ⁷⁴as har en atommasse på cirka 73.9238 amu.
* overflod:
* ⁷⁵as er den mere rigelige isotop, der udgør ca. 100% af naturligt forekommende arsen.
* ⁷⁴as er en sporingsisotop med en overflod på mindre end 1%.
Bemærk: Mens begge isotoper er kemisk identiske (de har det samme antal protoner og elektroner), kan forskellen i neutroner påvirke deres stabilitet og henfaldsegenskaber. For eksempel nogle radioaktive isotoper af arsenisk forfald gennem beta -emission, hvor en neutron omdannes til en proton, der ændrer elementet til selen.
Sidste artikelHvad er forskellen mellem akrylvandsbase og polymermaling?
Næste artikelHvad er de smagende undersystemer?
 Varme artikler
Varme artikler
-
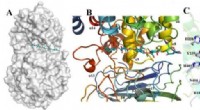 Strukturer i tang kaster lys over bæredygtighedOverfladerepræsentation og substratbindingsrille på Dp0100 Kredit:JI Shiqi Brunalger er ikke bare tang, der flyder i havet og floker svømmernes fødder - de indeholder også en hemmelighed. I sin ce
Strukturer i tang kaster lys over bæredygtighedOverfladerepræsentation og substratbindingsrille på Dp0100 Kredit:JI Shiqi Brunalger er ikke bare tang, der flyder i havet og floker svømmernes fødder - de indeholder også en hemmelighed. I sin ce -
 Identifikation af det mørke stof i den molekylære verdenKredit:CC0 Public Domain Forestil dig, at dit Facebook-feed udgør et fristende puslespil. Du bliver præsenteret for et par fragmenter om en person - øjenfarve, hårfarve, alder, og højde – og har k
Identifikation af det mørke stof i den molekylære verdenKredit:CC0 Public Domain Forestil dig, at dit Facebook-feed udgør et fristende puslespil. Du bliver præsenteret for et par fragmenter om en person - øjenfarve, hårfarve, alder, og højde – og har k -
 Lagring af energi med æggeskallerÆggeskaller består af porøst calciumcarbonat, der er særdeles velegnet til brug i elektrokemiske opbevaringssystemer. Kredit:Manuel Balzer, SÆT Bioaffald i form af hønseæggeskaller har vist sig at
Lagring af energi med æggeskallerÆggeskaller består af porøst calciumcarbonat, der er særdeles velegnet til brug i elektrokemiske opbevaringssystemer. Kredit:Manuel Balzer, SÆT Bioaffald i form af hønseæggeskaller har vist sig at -
 Vandbehandling - ny metode eliminerer hormonerMetoden udviklet af KIT kombinerer fordelene ved at binde mikroforurenende stoffer med aktivt kul med fordelene ved ultrafiltrering. Kredit:Sandra Göttisheim, SÆT Hormoner og andre mikroforurenend
Vandbehandling - ny metode eliminerer hormonerMetoden udviklet af KIT kombinerer fordelene ved at binde mikroforurenende stoffer med aktivt kul med fordelene ved ultrafiltrering. Kredit:Sandra Göttisheim, SÆT Hormoner og andre mikroforurenend
- Lys tænkning fører til gennembrud inden for detektion af nuklear trussel
- Parasitter fra husdyr, der påvirker dyrelivet verden over
- Fysikere springer acceleratorer med kosmiske stråler med ultrahøj energi
- Erindring om tidligere ting har indflydelse på, hvordan kvindelige feltkyllinger vælger kammerater…
- Nationalparker er smukke, men nøjsomhed og ulighed forhindrer mange i at nyde dem
- Video:Hvorfor antarktiske fisk ikke fryser ihjel


