Hvorfor er calcium højere end natrium i elektrokemisk serie?
Her er sammenbruddet:
* Elektrokemisk serie: Denne serie viser elementer (primært metaller) baseret på deres tendens til at få elektroner (reduktion) eller miste elektroner (oxidation).
* reduktionspotentiale: Et mål for, hvor sandsynligt et element er at vinde elektroner og blive en negativt ladet ion.
* mere negativ reduktionspotentiale =lettere oxidation: Elementer med mere negative reduktionspotentialer er lettere at oxidere (mister elektroner).
I den elektrokemiske serie har calcium et mere negativt reduktionspotentiale end natrium. Dette betyder, at calcium lettere oxideres end natrium. Her er hvorfor:
* atomstruktur: Calcium har to valenselektroner, mens natrium kun har en. Dette gør det lettere for calcium at miste elektroner og blive en +2 ion.
* Elektrostatisk attraktion: Den større størrelse af calciumens +2 -ion sammenlignet med natriumens +1 -ion fører til svagere elektrostatisk tiltrækning mellem kationen og dens elektroner.
Så selvom det ikke er strengt korrekt at sige, at calcium er "højere" end natrium, er det mere nøjagtigt at sige, at calcium har et mere negativt reduktionspotentiale og derfor lettere oxideres.
Fortæl mig, hvis du har flere spørgsmål!
Sidste artikelHvad er den rækkefølge, din krop bruger tre organiske forbindelser?
Næste artikelHvad er den letteste gas i luft?
 Varme artikler
Varme artikler
-
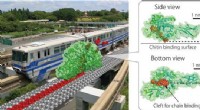 Chitinase som brændt bro, Brownsk monorail, der effektivt hydrolyserer genstridig biomasseFiktivt billede af en milliard gange forstørret SmChiA, der bevæger sig på krystallinsk kitin-lignende monorail-vogn (venstre panel) og kitin-bindende overflade og kløft af SmChiA (højre panel). SmChi
Chitinase som brændt bro, Brownsk monorail, der effektivt hydrolyserer genstridig biomasseFiktivt billede af en milliard gange forstørret SmChiA, der bevæger sig på krystallinsk kitin-lignende monorail-vogn (venstre panel) og kitin-bindende overflade og kløft af SmChiA (højre panel). SmChi -
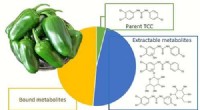 Peberplante suger antibiotika til personlig plejeproduktKredit:American Chemical Society Det kan nogle gange være svært at finde tandpasta, sæber og andre toiletartikler uden antibiotika. Deres popularitet har forårsaget en stigning i miljøniveauer af
Peberplante suger antibiotika til personlig plejeproduktKredit:American Chemical Society Det kan nogle gange være svært at finde tandpasta, sæber og andre toiletartikler uden antibiotika. Deres popularitet har forårsaget en stigning i miljøniveauer af -
 Forskere udvikler katalysator, der efterligner fotosyntesens Z-skemaCu2O (til højre), der gennemgår fotokorrosion i forhold til Cu2O/TiO2 (til venstre), der fungerer under en Z-ordning for at reducere CO2. Kredit:Ruixin Zhou Et team af kemikere fra University of K
Forskere udvikler katalysator, der efterligner fotosyntesens Z-skemaCu2O (til højre), der gennemgår fotokorrosion i forhold til Cu2O/TiO2 (til venstre), der fungerer under en Z-ordning for at reducere CO2. Kredit:Ruixin Zhou Et team af kemikere fra University of K -
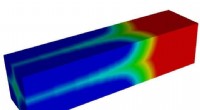 Undersøgelse afslører ukendte detaljer om almindelige lithium-ion batterimaterialerEn illustration viser væksten af en lithium-mangel fase (blå) på bekostning af en lithium-rig fase (rød) i en lithium jernfosfat mikrostav. Rice University-forskere ledede en undersøgelse, der fandt
Undersøgelse afslører ukendte detaljer om almindelige lithium-ion batterimaterialerEn illustration viser væksten af en lithium-mangel fase (blå) på bekostning af en lithium-rig fase (rød) i en lithium jernfosfat mikrostav. Rice University-forskere ledede en undersøgelse, der fandt
- Hvad var de første elementer, der findes i periodisk tabel?
- Sådan gør du eksponenter udenfor Parenthesis
- Hvad hedder elektrondonormolekylet?
- Amazons robotter:Jobødelæggere eller dansepartnere?
- AT&T foretager ændringer som reaktion på aktivistiske investorers fremstød
- SmokeBot – en robot, der betjener redningsenheder


