Chitinase som brændt bro, Brownsk monorail, der effektivt hydrolyserer genstridig biomasse
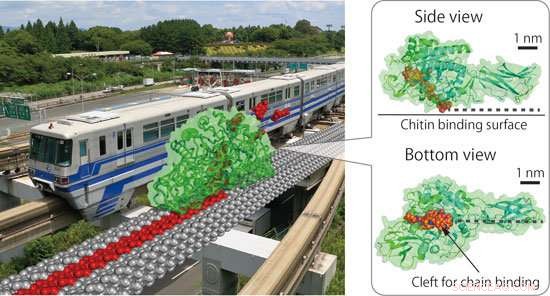
Fiktivt billede af en milliard gange forstørret SmChiA, der bevæger sig på krystallinsk kitin-lignende monorail-vogn (venstre panel) og kitin-bindende overflade og kløft af SmChiA (højre panel). SmChiA bevæger sig sammen med en enkelt kæde af chitin (vist med rødt) og skærer chitinet (skinnen) i opløselige disaccharider. Kredit:NINS/IMS
Molekylærmotorer omdanner energi til ensrettet mekanisk bevægelse. De fleste biomolekylære motorer i celler bruger adenosintrifosfat (ATP) som en kemisk energikilde. For nylig, imidlertid, Serratia marcescens chitinase A (SmChiA) er blevet genopdaget som en molekylær motor, der arbejder i ekstracellulære miljøer uden brug af ATP. Svarende til en monorail-vogn (fig. 1), SmChiA har spaltelignende polysaccharidbindingssteder og hydrolyserer processivt genstridigt krystallinsk chitin, en vigtig biomassekilde, til et vandopløseligt disaccharid chitobiose. Som et værktøj til omdannelse af biomasse til nyttige kemikalier, SmChiA er blevet grundigt undersøgt.
Under den processive katalyse og bevægelse på en krystallinsk kitinoverflade, SmChiA binder med en enkelt chitinkæde i den katalytiske kløft og gentager kemiske og mekaniske trin. I det kemiske trin, glykosidbindingen spaltes først, og substratets mellemstruktur hydrolyseres. Reaktionsproduktet, chitobiose, frigives derefter, og den næste chitobioseenhed skrælles fra krystaloverfladen (dekrystallisation) ledsaget af det fremadgående trin. I betragtning af størrelsen af reaktionsproduktet chitobiose (~1 nm), SmChiA forventes at bevæge sig med enkelt-nanometer trinstørrelser. Derfor, en enkelt-molekyle billeddannelsesteknik med høj præcision og hastighed var påkrævet for at løse de enkelte trin kombineret med katalyse.
For at forstå driftsmekanismen for hurtig katalyse og den ensrettede bevægelse af SmChiA, Nakamura og kolleger i Institut for Molekylær Videnskab (IMS) analyserede elementære bevægelsestrin kombineret med katalyse ved hjælp af højpræcision og højhastigheds enkeltmolekyle-billeddannelse sonderet med guldnanopartikler. De bekræftede hurtig ensrettet bevægelse (~50 nm s-1) med 1 nm fremad- og tilbageskridt, i overensstemmelse med længden af reaktionsproduktet chitobiose. Analyse af den kinetiske isotopeffekt afslørede, at hydrolyse er meget hurtigere end dekrystallisation. Det meget større frem-til-bagud-trinforhold forklares af konkurrencen mellem katalysen (86 procent) og baglæns bevægelse (14 procent), hvilket indikerer, at bevægelsen rettes fremad ved hurtig katalyse (fig. 2). Dette er den såkaldte "brændte bro"-mekanisme, fjernelse af skinnen bagved, og tvinger molekylet til at bevæge sig fremad.
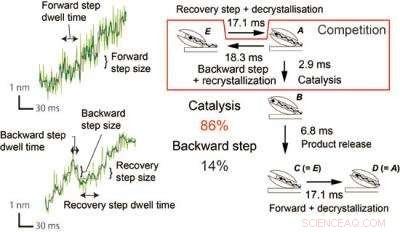
SmChiA viser 1-nm fremad, baglæns, og genopretningstrin af bevægelse (venstre). Forholdet mellem katalyse og tilbageskridt beregnet ud fra tidskonstanter var 86 procent og 14 procent, henholdsvis, hvilket indikerer hurtig katalyse, korrigerer den Brownske bevægelse langs chitinkæden (højre). Kredit:NINS/IMS
Desuden, gennem samarbejdet mellem IMS og Tokyo Institute of Technology, SmChiA viste sig at være en "brændt bro" Brownsk skralde, verificeret ved røntgenkrystallografi og molekylær dynamik simulering af de mellemliggende strukturer under glidende bevægelse. Dekrystallisering af en enkelt chitinkæde er det hastighedsbegrænsende bevægelsestrin, der opnås ved at binde fri energi på produktbindingsstedet, angivet ved sammenligning af fri energiforskelle estimeret ved enkeltmolekyleanalyse med krystallinsk kitin og teoretisk beregning af bindingsenergien med opløseligt oligo-saccharid.
Fundet demonstrerer, hvordan SmChiA kontrollerer den Brownske bevægelse og udvinder hurtig ensrettet bevægelse for kontinuerlig nedbrydning af krystallinsk kitin uden dissociation. Strategien udviklet af SmChiA kan ikke kun anvendes til at udvikle chitinaser og cellulaser til mere effektive nedbrydninger af kitin og cellulose, men også at designe hurtigt bevægende kunstige molekylære motorer såsom DNA walkers.
 Varme artikler
Varme artikler
-
 En ny energibesparende LED-fosforKrystalstrukturen af SALON-fosforen er årsagen til dens fremragende luminescensegenskaber. Kredit:University of Innsbruck Det menneskelige øje er særligt følsomt over for grønt, men mindre følso
En ny energibesparende LED-fosforKrystalstrukturen af SALON-fosforen er årsagen til dens fremragende luminescensegenskaber. Kredit:University of Innsbruck Det menneskelige øje er særligt følsomt over for grønt, men mindre følso -
 Molekylært mål UNC45A er afgørende for cancer, men ikke normal celleproliferationDr. Ahmed Chadli. Kredit:Phil Jones, Seniorfotograf, Augusta University Identifikation af et protein, der spiller en nøglerolle i kræftcellevækst, er et første skridt mod udviklingen af en målre
Molekylært mål UNC45A er afgørende for cancer, men ikke normal celleproliferationDr. Ahmed Chadli. Kredit:Phil Jones, Seniorfotograf, Augusta University Identifikation af et protein, der spiller en nøglerolle i kræftcellevækst, er et første skridt mod udviklingen af en målre -
 Et komplet sæt energiniveaupositioner for alle primære metalhalogenidperovskitterKredit:Eindhoven University of Technology Metalhalogenidperovskitter udgør en populær klasse af materialer med spændende optoelektroniske egenskaber. En grundlæggende forståelse af variationerne i
Et komplet sæt energiniveaupositioner for alle primære metalhalogenidperovskitterKredit:Eindhoven University of Technology Metalhalogenidperovskitter udgør en populær klasse af materialer med spændende optoelektroniske egenskaber. En grundlæggende forståelse af variationerne i -
 Kasseret affald kan være en skatkammer af sjældne metallerMagnetiske felter er blandt de teknikker, der udvikles til at udvinde metalpartikler fra slagger (stenet affaldsmateriale). Kredit:Slaggebunke ved Rammelsberg / Goslar af B.Nunold er licenseret under
Kasseret affald kan være en skatkammer af sjældne metallerMagnetiske felter er blandt de teknikker, der udvikles til at udvinde metalpartikler fra slagger (stenet affaldsmateriale). Kredit:Slaggebunke ved Rammelsberg / Goslar af B.Nunold er licenseret under
- Storbritannien har et højere niveau af regional ulighed end noget andet stort velhavende land
- Storstilet fase-hentning
- Risici ved at manipulere den globale termostat
- Meget effektiv køling ved hjælp af et nyt nanoporøst fast stof
- Simple & Easy Science Fair Projects
- Et nyt nanoaktuatorsystem er blevet udviklet


