Hvordan kan en kemiske reaktioner, der bruges i vand?
1. Vandoprensning:
* koagulation og flokkulering: Kemikalier som aluminiumssulfat (alun) tilsættes til vand for at danne klæbrige flokke, der fanger urenheder som snavs og bakterier, hvilket gør dem lettere at fjerne.
* desinfektion: Klor eller ozon bruges til at dræbe skadelige bakterier og vira, hvilket sikrer sikkert drikkevand.
* Vandblødgøring: Lime- eller natriumcarbonat tilsættes for at fjerne calcium- og magnesiumioner (hårdhed) fra vand, hvilket forhindrer mineralopbygning i rør.
2. Aquatic Life:
* Fotosyntese: Alger og akvatiske planter bruger sollys, kuldioxid og vand til at producere ilt og glukose. Dette er grundlaget for fødevarekæden i vandøkosystemer.
* respiration: Fisk og andre akvatiske organismer bruger ilt opløst i vand til at producere energi og frigive kuldioxid. Dette er det modsatte af fotosyntesen.
* Næringscykling: Bakterier spiller en vigtig rolle i at nedbryde organisk stof i vand, hvilket frigiver næringsstoffer som nitrogen og fosfor tilbage i økosystemet.
3. Industrielle processer:
* Elektrolyse af vand: Ved hjælp af elektricitet opdeles vand i brint og iltgas. Dette har applikationer inden for brændstofproduktion og kemisk fremstilling.
* Kemisk syntese: Vand tjener som opløsningsmiddel og reaktant i adskillige kemiske reaktioner, herunder produktion af gødning, farmaceutiske stoffer og andre materialer.
4. Miljøprocesser:
* sur regn: Svovldioxid og nitrogenoxider frigivet ved forbrænding af fossile brændstoffer reagerer med vanddamp i atmosfæren og danner svovlsyrer og salpetersyrer, der falder som surt regn og beskadiger økosystemer.
* eutrofiering: Overskydende næringsstoffer som fosfor og nitrogen fra landbrugsafstrømning reagerer i vand, hvilket fører til algeopblomstringer, der udtømmer ilt og skadelig akvatisk liv.
5. Hverdag:
* rengøring: Mange rengøringsprodukter er afhængige af kemiske reaktioner i vand for at nedbryde fedt, snavs og pletter.
* Madlavning: Vand er en nøgleingrediens i mange madlavningsprocesser, der deltager i kemiske reaktioner, der blødgør mad og skaber nye smag.
Eksempler på specifikke kemiske reaktioner:
* neutralisering: Syrer og baser reagerer i vand for at danne salte og vand, som reaktionen af saltsyre (HCI) med natriumhydroxid (NaOH) til dannelse af natriumchlorid (NaCl) og vand (H2O).
* Oxidationsreduktion: Mange reaktioner i vand involverer overførsel af elektroner, ligesom rusten af jern, hvor jernatomer mister elektroner til ilt.
* nedbør: Visse kemikalier reagerer i vand for at danne uopløselige faste stoffer, som reaktionen af calciumioner med carbonationer til dannelse af calciumcarbonat (CACO3), som er en almindelig komponent i kalksten.
Generelt er kemiske reaktioner i vand afgørende for en lang række naturlige og menneskedrevne processer, der spiller en vigtig rolle i alt fra rensende drikkevand til at opretholde helbredet på vores planet.
Sidste artikelHvordan er temperaturen på en gas relateret til bevægelsesmolekyler?
Næste artikelAtomnummer beskriver hvad?
 Varme artikler
Varme artikler
-
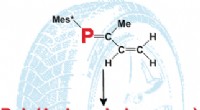 En kemisk funktionel fosforversion af naturgummiGoodyears opdagelse i 1839 af vulkaniseringen af naturgummi opnået fra gummitræer markerer begyndelsen på den moderne gummiindustri. En række syntetiske gummiprodukter blev efterfølgende udviklet. I
En kemisk funktionel fosforversion af naturgummiGoodyears opdagelse i 1839 af vulkaniseringen af naturgummi opnået fra gummitræer markerer begyndelsen på den moderne gummiindustri. En række syntetiske gummiprodukter blev efterfølgende udviklet. I -
 Seneste fremskridt i faststof-NMR-undersøgelser af zeolitkatalysatorer(a) 2D refokuseret UTIDSÆSTLIGT (J-medieret) 29Si{29Si} DQ NMR-spektrum af as-syntetiseret zeolit ITW. (b) DNP-forstærket 2D 29Si{29Si} J-medieret korrelationsspektrum af calcineret Si-SSZ-70. (c) S
Seneste fremskridt i faststof-NMR-undersøgelser af zeolitkatalysatorer(a) 2D refokuseret UTIDSÆSTLIGT (J-medieret) 29Si{29Si} DQ NMR-spektrum af as-syntetiseret zeolit ITW. (b) DNP-forstærket 2D 29Si{29Si} J-medieret korrelationsspektrum af calcineret Si-SSZ-70. (c) S -
 Forskere testede med succes ny vandsimuleringsprotokolDen justerede protokol giver en klar forbedring af forståelsen mellem de forskellige tilgange til simulering. Her, den justerede protokol i brug (sort) og teori (rød) for massetæthedsudsving under båd
Forskere testede med succes ny vandsimuleringsprotokolDen justerede protokol giver en klar forbedring af forståelsen mellem de forskellige tilgange til simulering. Her, den justerede protokol i brug (sort) og teori (rød) for massetæthedsudsving under båd -
 Hudvaccination med mikronåleplaster, influenzafusionsprotein forbedrer effektiviteten af influenz…Kredit:Georgia State University En boostende hudvaccination med et bionedbrydeligt mikronåleplaster og protein konstrueret ud fra sekvenser af influenzavirus undertyper kunne forbedre effektivitet
Hudvaccination med mikronåleplaster, influenzafusionsprotein forbedrer effektiviteten af influenz…Kredit:Georgia State University En boostende hudvaccination med et bionedbrydeligt mikronåleplaster og protein konstrueret ud fra sekvenser af influenzavirus undertyper kunne forbedre effektivitet
- Forskere foreslår en ny type planetobjekt
- Forskellen mellem Bobcat & Coyote Tracks
- Når du køber online, kunder foretrækker live chat frem for telefonopkald
- Klistermærke gør lysmanipulation i nanoskala nemmere at fremstille
- Hvad er økologiske konkurrencer kaffepicienter?
- Substitutionsdoping af 2D-halvleder til bredbåndsfotodetektor


