Hvilken type reaktion er mest afhængig af koncentrationsprodukter eller reaktanter?
Her er hvorfor:
* reversible reaktioner kan fortsætte i både de forreste og omvendte retninger.
* ligevægtsposition af en reversibel reaktion (de relative mængder produkter og reaktanter ved ligevægt) bestemmes af hastighedskonstanter For de fremadgående og omvendte reaktioner.
* Disse hastighedskonstanter påvirkes af koncentrationen af reaktanter og produkter.
for eksempel:
Overvej reaktionen:
A + B ⇌ C + D
* Hvis koncentrationen af reaktanter (A og B) er høj, fremadrettet reaktion vil blive foretrukket, hvilket fører til en højere koncentration af produkter (C og D).
* Hvis koncentrationen af produkter (C og D) er høj, omvendt reaktion vil blive foretrukket, hvilket fører til en højere koncentration af reaktanter (A og B).
Derfor er ligevægtspositionen for en reversibel reaktion meget følsom over for ændringer i koncentrationerne af reaktanter og produkter. Dette er grunden til, at reversible reaktioner betragtes som de mest afhængige af koncentration.
Sidste artikelHvilket element har tre isotoper forskellige navne?
Næste artikelI hvilken type substitueret kulbrinte kan klor være atomet?
 Varme artikler
Varme artikler
-
 Gamle enzymer katalysatorer for nye opdagelser(L-R) Elizabeth Gillam og Jong-Min (Joseph) Baek ser på P450 enzymspektre på et specialiseret spektrofotometer, vurdere om proteinet er intakt eller inaktivt. Kredit:University of Queensland Forsk
Gamle enzymer katalysatorer for nye opdagelser(L-R) Elizabeth Gillam og Jong-Min (Joseph) Baek ser på P450 enzymspektre på et specialiseret spektrofotometer, vurdere om proteinet er intakt eller inaktivt. Kredit:University of Queensland Forsk -
 Forskere afslører strukturen af aminosyretransportør involveret i kræftForskere fra University of Groningen involveret i undersøgelsen - venstre til højre, stående:D.J. Slotboom, A. Guskov, A.A. Garaeva, C. Paulino - siddende:G.T. Oostergetel. Kredit:University of Gronin
Forskere afslører strukturen af aminosyretransportør involveret i kræftForskere fra University of Groningen involveret i undersøgelsen - venstre til højre, stående:D.J. Slotboom, A. Guskov, A.A. Garaeva, C. Paulino - siddende:G.T. Oostergetel. Kredit:University of Gronin -
 Hvidvin, citronsaft combo forhindrer uønsket misfarvning af wienerbrødsdejKredit:CC0 Public Domain Lige meget om det er bedstemors småkager eller kommercielt fremstillede rundstykker, wienerbrød elskere forventer, at deres bagværk har en vis gyldenbrun tiltrækning - men
Hvidvin, citronsaft combo forhindrer uønsket misfarvning af wienerbrødsdejKredit:CC0 Public Domain Lige meget om det er bedstemors småkager eller kommercielt fremstillede rundstykker, wienerbrød elskere forventer, at deres bagværk har en vis gyldenbrun tiltrækning - men -
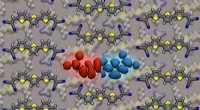 Tuning the energy gap:En ny tilgang til organiske halvledereVarierende forholdet mellem 3T -molekyler (forgrund) og 6T -molekyler (angivet i baggrunden) i blandingen gør det muligt at afstemme hullet kontinuerligt. Kredit:Sebastian Hutsch, Frank Ortmann Tu
Tuning the energy gap:En ny tilgang til organiske halvledereVarierende forholdet mellem 3T -molekyler (forgrund) og 6T -molekyler (angivet i baggrunden) i blandingen gør det muligt at afstemme hullet kontinuerligt. Kredit:Sebastian Hutsch, Frank Ortmann Tu
- Er nogle ting, vi genbruger, bedre stillet på lossepladser?
- Kunne de samme laboratorieteknikker, der blev brugt til at fremstille syntetiske perler, være sedim…
- Månens faser Aktiviteter for børn
- Ashkenaziske jøders mystiske oprindelse optrevlet af videnskabsmænd takket være gammelt DNA
- Når klipper er på en så stor dybde, smelter de faktisk på grund af?
- Kemi løser giftige bekymringer omkring kulnanorør


