Har ædle gasser en fuld oktet elektroner?
Her er hvorfor:
* octet regel: Octet -reglen siger, at atomer har en tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration af otte elektroner i deres yderste energiniveau (Valence Shell).
* ædle gaskonfiguration: Noble gasser har allerede otte elektroner i deres valensskal (undtagen helium, der har to). Dette gør dem meget stabile og ureaktive, da de ikke har behov for at vinde, miste eller dele elektroner.
Eksempel:
* neon (NE): Har 10 elektroner med konfigurationen 2, 8 (to i den første skal og otte i den anden skal). Dette er en fuld octet.
* helium (He): Har 2 elektroner med konfigurationen 2.. Dette er en fuld duet, som er den stabile konfiguration for det første energiniveau.
På grund af deres stabile elektronkonfigurationer kaldes ædle gasser ofte "inerte gasser". Det er dog vigtigt at bemærke, at nogle ædle gasser kan deltage i kemiske reaktioner under specifikke forhold.
Sidste artikelHvilken subatomisk partikel har en positiv ladning, hvor i atomet?
Næste artikelHvad er nogle hydrolyserbare lipider?
 Varme artikler
Varme artikler
-
 At gøre katalytiske overflader mere aktive for at hjælpe med at dekarbonisere brændstoffer og kem…Kredit:Massachusetts Institute of Technology Elektrokemiske reaktioner, der accelereres ved hjælp af katalysatorer, er kernen i mange processer til fremstilling og brug af brændstoffer, kemikalier
At gøre katalytiske overflader mere aktive for at hjælpe med at dekarbonisere brændstoffer og kem…Kredit:Massachusetts Institute of Technology Elektrokemiske reaktioner, der accelereres ved hjælp af katalysatorer, er kernen i mange processer til fremstilling og brug af brændstoffer, kemikalier -
 Proteinkæder, der selv dannes til spiralformede fletningerSEM-mikrofotografier af fletningstopologier observeret i geler af 2. a, Tegneseriediagrammer, der viser tostrengede sammenfiltringer og deres tilsvarende flettede ord. Fletningsordet beskriver mønster
Proteinkæder, der selv dannes til spiralformede fletningerSEM-mikrofotografier af fletningstopologier observeret i geler af 2. a, Tegneseriediagrammer, der viser tostrengede sammenfiltringer og deres tilsvarende flettede ord. Fletningsordet beskriver mønster -
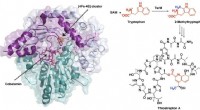 Syntese af potent antibiotikum følger en usædvanlig kemisk vejSyntesen af det potente antibiotikum thiostrepton bruger et radikalt SAM-protein TsrM, hvis krystalstruktur er vist til venstre, mens den er bundet til en jern-svovl-klynge og cobalamin. Nye billede
Syntese af potent antibiotikum følger en usædvanlig kemisk vejSyntesen af det potente antibiotikum thiostrepton bruger et radikalt SAM-protein TsrM, hvis krystalstruktur er vist til venstre, mens den er bundet til en jern-svovl-klynge og cobalamin. Nye billede -
 Ny udskrivningsproces fremmer 3-D-kapaciteterDette trækobjekt blev skabt ved hjælp af 3D-injektionsprint, en ny teknologi opfundet af UMass Lowell Plastics Engineering Prof. David Kazmer. Kredit:David Kazmer Mere holdbare proteser og medicin
Ny udskrivningsproces fremmer 3-D-kapaciteterDette trækobjekt blev skabt ved hjælp af 3D-injektionsprint, en ny teknologi opfundet af UMass Lowell Plastics Engineering Prof. David Kazmer. Kredit:David Kazmer Mere holdbare proteser og medicin
- Hvad er betydningen af virtual reality for læger og kirurger?
- Photodetektion på chip:Todimensionelle materiale-heterojunctions
- Astronomer observerer Radcliffe-bølgen svinge
- Få realistiske scenarier tilbage for at begrænse den globale opvarmning til 1,5 ° C
- Fødevarepriser til forbrugere i etniske enklaver kan forklare forskel i assimileringshastigheder
- David Attenborough får ny artsnavnebror


