Når mættede opløsninger er de normalt umættede?
* Definition: En mættet opløsning indeholder den maksimale mængde opløst stof, der kan opløses ved en given temperatur og tryk. Eventuelle ekstra opløselige tilføjede vil simpelthen slå sig ned i bunden.
* ligevægt: Mættede opløsninger er i en ligevægtstilstand. Dette betyder, at opløsningshastigheden er lig med krystallisationshastigheden. Løsningen forsøger konstant at opretholde denne balance.
* Faktorer: For at få en mættet opløsning til at blive umættet, skal du ændre forholdene. Her er nogle måder:
* Forøg temperaturen: For de fleste faste stoffer vil øge temperaturen øge opløseligheden af opløseligheden. Dette gør det muligt for løsningen at holde mere opløst og blive umættet.
* Faldstemperatur: For de fleste faste stoffer vil reducere temperaturen reducere opløseligheden af opløseligheden. Dette kan få noget af det opløste stof til at udfælde ud af opløsningen, hvilket gør det umættet.
* Fjern opløsningsmiddel: Hvis du fjerner noget af opløsningsmidlet (som vand), øges koncentrationen af opløstelsen. Dette kan gøre opløsningen mættet eller endda overmættet, hvis den overstiger opløselighedsgrænsen.
* Tilføj mere opløsningsmiddel: Tilsætning af mere opløsningsmiddel vil fortynde opløsningen og sænke koncentrationen af opløstelsen. Dette vil gøre løsningen umættet.
Kortfattet: Mættede opløsninger forbliver mættede, medmindre forholdene ændres for at skifte ligevægt.
Sidste artikelHvordan udtrykker du opløselighed?
Næste artikelHvordan adskiller du en blanding af saltvand og sand får stadig vand?
 Varme artikler
Varme artikler
-
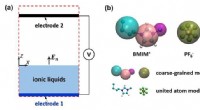 Forskning forbedrer ionfordampningsteorier og ydeevne af elektrosprayapplikationerSkematisk af simuleringssystemet for molekylær dynamik (MD). (til højre) To modeller af BMIM, PF6 bruges i MD -simuleringer. Kredit:JIANG Xikai Elektrospray af ioniske væsker ved stuetemperatur (R
Forskning forbedrer ionfordampningsteorier og ydeevne af elektrosprayapplikationerSkematisk af simuleringssystemet for molekylær dynamik (MD). (til højre) To modeller af BMIM, PF6 bruges i MD -simuleringer. Kredit:JIANG Xikai Elektrospray af ioniske væsker ved stuetemperatur (R -
 Enzymcocktail udviklet i Brasilien driver produktionen af anden generations ethanolTrichoderma reesei svamp RUT-C30 stamme, som blev konstrueret til at producere enzymer med højt udbytte. Kredit:LNBR-CNPEM Forskere ved det brasilianske center for forskning i energi og materialer
Enzymcocktail udviklet i Brasilien driver produktionen af anden generations ethanolTrichoderma reesei svamp RUT-C30 stamme, som blev konstrueret til at producere enzymer med højt udbytte. Kredit:LNBR-CNPEM Forskere ved det brasilianske center for forskning i energi og materialer -
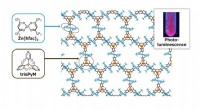 En ny opskrift på luftstabil og højkrystallinsk radikalbaseret koordinationspolymerEn 2D honeycomb gitterstruktur af en radikal-baseret koordinationspolymer, trisZn, konstrueret af trisPyM og Zn(hfac) 2 . Fotoluminescens fra trisZn er vist. Kredit:NINS/IMS Koordinationspolymer
En ny opskrift på luftstabil og højkrystallinsk radikalbaseret koordinationspolymerEn 2D honeycomb gitterstruktur af en radikal-baseret koordinationspolymer, trisZn, konstrueret af trisPyM og Zn(hfac) 2 . Fotoluminescens fra trisZn er vist. Kredit:NINS/IMS Koordinationspolymer -
 Kemikere syntetiserer millioner af proteiner, der ikke findes i naturenZachary P. Gates (til venstre) og Brad Pentelute med deres ætsning af Xenoprotein. Kredit:Rachael Fuller MIT-kemikere har udtænkt en måde til hurtigt at syntetisere og screene millioner af nye pro
Kemikere syntetiserer millioner af proteiner, der ikke findes i naturenZachary P. Gates (til venstre) og Brad Pentelute med deres ætsning af Xenoprotein. Kredit:Rachael Fuller MIT-kemikere har udtænkt en måde til hurtigt at syntetisere og screene millioner af nye pro
- Hvad beskriver bevægelsen af vandmolekyle i is?
- Borgerforsker -dykkere kaster lys over virkningen af opvarmende oceaner på havlivet
- Hvad giver kobberbromid og natriumsulfat?
- Få dit lægemiddel nano-leveret via mikroboble
- Er elodea og cattail vandplanter?
- Disney profiterer, da Fox slutter sig til folden


