I batteri en kemisk reaktion mellem hvilke to metaller producerede strøm?
* metaller :Som zink og kobber i et simpelt batteri.
* metallegeringer :Kombinationer af metaller.
* Andre ledende materialer :Som kulstof, grafit eller endda visse metaloxider.
Sådan fungerer det:
1. Elektroder: Batteriet indeholder to elektroder, en anode (negativ) og A katode (positiv).
2. elektrolyt: Elektroderne er nedsænket i en elektrolyt , en løsning, der leder elektricitet. Denne opløsning kan være en syre, base eller et salt.
3. Kemisk reaktion: En kemisk reaktion forekommer mellem elektroderne og elektrolytten. Denne reaktion får elektroner til at strømme fra anoden til katoden gennem et eksternt kredsløb.
4. strømstrøm: Bevægelsen af disse elektroner skaber en elektrisk strøm, der kan strømenheder.
Forenklet eksempel:
I et simpelt batteri, som et zink-kobberbatteri, involverer den kemiske reaktion:
* anode (zink): Zinkatomer mister elektroner og bliver zinkioner (Zn²⁺). Disse ioner opløses i elektrolytten.
* katode (kobber): Kobberioner i elektrolytten får elektroner og bliver kobberatomer, der pletteres på kobberelektroden.
Denne strøm af elektroner fra anoden til katoden skaber den elektriske strøm.
Nøglepunkt: De specifikke metaller, der bruges i et batteri, bestemmer spændingen og andre egenskaber ved batteriet.
Sidste artikelHvor mange gram lidocaine er i 150 ml en 2,5 m opløsning?
Næste artikelHvilke metalioner brænder med en orange flamme?
 Varme artikler
Varme artikler
-
 Lægemiddelinducerede cellulære membrankomplekser inducerer cancercelledødOgretmen, vist her i hans laboratorium på Hollings Cancer Center, siger, at disse indledende fund er et positivt skridt i søgen efter mere effektive kræftlægemidler. Kredit:Emma Vought Gamle molek
Lægemiddelinducerede cellulære membrankomplekser inducerer cancercelledødOgretmen, vist her i hans laboratorium på Hollings Cancer Center, siger, at disse indledende fund er et positivt skridt i søgen efter mere effektive kræftlægemidler. Kredit:Emma Vought Gamle molek -
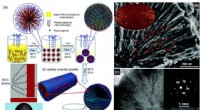 Hierarkisk mesoporøse titaniumdioxidmaterialer til energi- og miljøanvendelserSkematisk fremstilling af dannelsesprocessen for hierarkisk mesoporøse TiO2-mikrosfærer med enkeltkrystallignende porevæg gennem fordampningsdrevet orienteret samling (a). SEM-billede af en enkelt ult
Hierarkisk mesoporøse titaniumdioxidmaterialer til energi- og miljøanvendelserSkematisk fremstilling af dannelsesprocessen for hierarkisk mesoporøse TiO2-mikrosfærer med enkeltkrystallignende porevæg gennem fordampningsdrevet orienteret samling (a). SEM-billede af en enkelt ult -
 Nye bioinspirerede hydrogeler kan fungere som superlim i meget ioniske miljøer som havvandDen nyudviklede gel klæber til negativt ladede faste overflader under meget ioniske forhold, såsom i havvand. Kredit:Hailong Fan et al., Naturkommunikation, 12. november kl. 2019 Forskere har arbe
Nye bioinspirerede hydrogeler kan fungere som superlim i meget ioniske miljøer som havvandDen nyudviklede gel klæber til negativt ladede faste overflader under meget ioniske forhold, såsom i havvand. Kredit:Hailong Fan et al., Naturkommunikation, 12. november kl. 2019 Forskere har arbe -
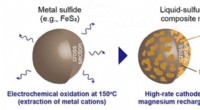 Genopladelige magnesiumbatterier med høj hastighed bevæger sig et skridt tættere på realiseringe…Skematisk illustration, der viser konceptet for dette arbejde. Flydende svovl/sulfid kompositmaterialer fremstillet ved elektrokemisk oxidation af metalsulfider kan fungere som højtydende katodemateri
Genopladelige magnesiumbatterier med høj hastighed bevæger sig et skridt tættere på realiseringe…Skematisk illustration, der viser konceptet for dette arbejde. Flydende svovl/sulfid kompositmaterialer fremstillet ved elektrokemisk oxidation af metalsulfider kan fungere som højtydende katodemateri
- Hvor dårlig forvaltning af nigerianske skove førte til udnyttelse af kriminelle
- At se det usete:Hvordan sommerfugle kan hjælpe forskere med at opdage kræft
- Håndtag og huller i abstrakte rum:Hvordan et materiale leder elektricitet bedre
- Påsketornado-trussel udgør et sikkerhedsdilemma under pandemi
- Hvad hører hjemme i det tomme rum i følgende kemiske ligning for afbrænding af fossilt brændstof…
- NASA finder en mindre langstrakt potentiel Tropical Cyclone Six


