Hvad sker der, når du tilføjer mere NH4CL til magnesiumhydroxid?
* ligevægt og Le Chatelier's princip: Magnesiumhydroxid er en lidt opløselig forbindelse, hvilket betyder, at det findes i ligevægt med dets ioner i opløsning:
Mg (OH) ₂ (s) ⇌ mg²⁺ (aq) + 2OH⁻ (aq)
* ammoniumchlorides rolle: Ammoniumchlorid er en stærk elektrolyt der dissocierer helt i løsning:
NH₄CL (aq) → NH₄⁺ (aq) + cl⁻ (aq)
Ammoniumionerne (NH₄⁺) reagerer med hydroxidionerne (OH⁻) fra magnesiumhydroxid -ligevægten:
NH₄⁺ (aq) + OH⁻ (aq) ⇌ NH₃ (aq) + h₂o (l)
Denne reaktion fjerner hydroxidioner Fra opløsningen, der skifter ligevægt af magnesiumhydroxidopløsningen til højre , der favoriserer opløsning af mere magnesiumhydroxid.
Kortfattet:
1. Tilsætning af NH₄CL øger koncentrationen af NH₄⁺ioner.
2. Disse ioner reagerer med OH⁻ioner fra magnesiumhydroxid -ligevægten.
3. denne reaktion fjerner OH⁻ -ioner, hvilket får ligevægten til at skifte til højre, hvilket favoriserer opløsningen af mere Mg (OH) ₂.
Resultat: Den samlede virkning er, at mere magnesiumhydroxid opløses i nærvær af ammoniumchlorid.
Sidste artikelHvad er brugen af 2 chlorethanol?
Næste artikelHvad er ikke -eksempler på Coriolis -effekt?
 Varme artikler
Varme artikler
-
 Kryo-elektronmikroskopi kaster nyt lys over batterierKredit:Kourkoutis Lab Grænsefladen mellem den faste anode og den flydende elektrolyt spiller en afgørende rolle i ydelsen af et lithium-metalbatteri, men karakterisering af de processer, der ske
Kryo-elektronmikroskopi kaster nyt lys over batterierKredit:Kourkoutis Lab Grænsefladen mellem den faste anode og den flydende elektrolyt spiller en afgørende rolle i ydelsen af et lithium-metalbatteri, men karakterisering af de processer, der ske -
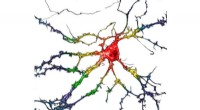 Forskere identificerer et psykedelisk lignende stof uden de hallucinogene bivirkningerEt repræsentativt billede af dyrkede dissocierede hippocampusneuroner, der midlertidigt udtrykker psychLight1 og psychLight2. Skala bar, 20 mm. Kredit:Calvin Ly Psykedeliske lægemidler har vist lø
Forskere identificerer et psykedelisk lignende stof uden de hallucinogene bivirkningerEt repræsentativt billede af dyrkede dissocierede hippocampusneuroner, der midlertidigt udtrykker psychLight1 og psychLight2. Skala bar, 20 mm. Kredit:Calvin Ly Psykedeliske lægemidler har vist lø -
 Computere deltager i kampen mod COVID-19Kredit:CC0 Public Domain Forskere overalt slår sig sammen for at bekæmpe den nye coronavirus, og de gør allerede fremskridt. Computation chemists er fokuseret på at bygge computermodeller af virus
Computere deltager i kampen mod COVID-19Kredit:CC0 Public Domain Forskere overalt slår sig sammen for at bekæmpe den nye coronavirus, og de gør allerede fremskridt. Computation chemists er fokuseret på at bygge computermodeller af virus -
 AI identificerer ændringer i mikrostruktur i aldrende materialerTopologisk analyse af røntgen-CT-data til genkendelse og trending af ændringer i mikrostruktur under materialeældning. Kredit:Lawrence Livermore National Laboratory Lawrence Livermore National Lab
AI identificerer ændringer i mikrostruktur i aldrende materialerTopologisk analyse af røntgen-CT-data til genkendelse og trending af ændringer i mikrostruktur under materialeældning. Kredit:Lawrence Livermore National Laboratory Lawrence Livermore National Lab
- Ny model afslører muligheden for at pumpe antibiotika ind i bakterier
- Er computeren en god model for hjernen?
- Forskere går sammen for at vise, at skovens biodiversitet er grøn på mere end én måde
- Undersøgelse:Demokratiske holdninger kan fortsætte i lande med svag regeringsførelse, selv under …
- Hvor mange hydrogenatomer findes i 2 molekyler hydroxylamin?
- Ny forskning viser, at mænd og kvinder fra Roman Herculaneum havde forskellige diæter


