Hvorfor opstår en dobbeltstatningsreaktion?
Det grundlæggende:
* dobbeltudskiftning: I en dobbeltstatningsreaktion udveksler to reaktanter (normalt ioniske forbindelser) deres kationer (positivt ladede ioner) for at danne to nye produkter.
Hvorfor sker det:
1. Dannelse af et bundfald: Den mest almindelige drivkraft til dobbeltudskiftning er dannelsen af en uopløselig forbindelse (et bundfald). Dette bundfald er mere stabilt end de originale reaktanter, og dens dannelse fjerner ioner fra opløsningen og driver reaktionen fremad.
2. Dannelse af en gas: En anden måde at opnå stabilitet på er dannelsen af en gas. Gassen slipper ud af opløsningen, fjerner den fra ligevægten og favoriserer produktdannelse.
3. Dannelse af vand: Vand er et meget stabilt molekyle, og dets dannelse er en almindelig drivkraft til dobbeltstatningsreaktioner. Dette gælder især i reaktioner, der involverer syrer og baser.
4. Dannelse af en svag elektrolyt: Hvis et af produkterne er en svag elektrolyt (en forbindelse, der ikke adskiller sig fuldstændigt i opløsning), kan reaktionen skifte til højre for at favorisere dens dannelse, da dette fører til et mindre stabilt produkt.
Eksempel:
Overvej reaktionen mellem sølvnitrat (Agno₃) og natriumchlorid (NaCl):
Agno₃ (aq) + NaCl (aq) → Agcl (s) + nano₃ (aq)
* drivkraft: Dannelse af et bundfald (AgCl, sølvchlorid)
* Forklaring: Sølvionerne (Ag⁺) og chloridioner (CL⁻) kombineres for at danne et stabilt, uopløseligt fast stof, fjerne dem fra opløsningen og føre reaktionen fremad.
Kortfattet:
Dobbeltudskiftningsreaktioner opnår en mere stabil tilstand. Dette kan opnås ved at danne et bundfald, en gas, vand eller en svag elektrolyt. Reaktionen favoriserer dannelsen af disse mere stabile produkter, hvilket fører til udveksling af ioner og oprettelsen af nye forbindelser.
Sidste artikelEr det typisk for overgangsmetaller at have isotoper?
Næste artikelHvad er brugen af 2 chlorethanol?
 Varme artikler
Varme artikler
-
 Materialeforskere finder en ny vinkel mod bedre varmeoverførselSilicium wafers belagt med gradient ENZ materialer set gennem et termisk billedkamera. Kredit:Raman Laboratory/UCLA UCLA-materialeforskere har udviklet en klasse af optisk materiale, der styrer, h
Materialeforskere finder en ny vinkel mod bedre varmeoverførselSilicium wafers belagt med gradient ENZ materialer set gennem et termisk billedkamera. Kredit:Raman Laboratory/UCLA UCLA-materialeforskere har udviklet en klasse af optisk materiale, der styrer, h -
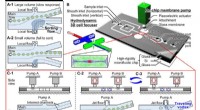 Banebrydende oprensning af fossilt pollen ved hjælp af en ny storpartikel-on-chip sortererKonceptuelle billeder af det foreslåede on-chip sorteringssystem for store partikler baseret på spatiotemporalt genererede rejsehvirvler. (A) Konceptuelle billeder af konventionel partikelsortering på
Banebrydende oprensning af fossilt pollen ved hjælp af en ny storpartikel-on-chip sortererKonceptuelle billeder af det foreslåede on-chip sorteringssystem for store partikler baseret på spatiotemporalt genererede rejsehvirvler. (A) Konceptuelle billeder af konventionel partikelsortering på -
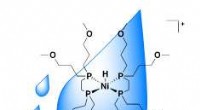 Ny nikkelkatalysator opererer i vand for at omdanne drivhusgas til kemisk råmaterialeNy nikkelkatalysator tilføjer hydrogen (H2) til kuldioxid (CO2) i vand ved hjælp af bikarbonat (NaHCO 3 ) som base. Propylethergrupperne på phosphinliganderne (lange kæder) gør nikkel (Ni)-katalysat
Ny nikkelkatalysator opererer i vand for at omdanne drivhusgas til kemisk råmaterialeNy nikkelkatalysator tilføjer hydrogen (H2) til kuldioxid (CO2) i vand ved hjælp af bikarbonat (NaHCO 3 ) som base. Propylethergrupperne på phosphinliganderne (lange kæder) gør nikkel (Ni)-katalysat -
 Ny proces indsnævrer kløften mellem naturlige og syntetiske materialerKredit:EPFL Naturmaterialer som hud, brusk og sener er hårde nok til at understøtte vores kropsvægt og bevægelser, alligevel fleksible nok til at de ikke revner let. Selvom vi tager disse ejendomm
Ny proces indsnævrer kløften mellem naturlige og syntetiske materialerKredit:EPFL Naturmaterialer som hud, brusk og sener er hårde nok til at understøtte vores kropsvægt og bevægelser, alligevel fleksible nok til at de ikke revner let. Selvom vi tager disse ejendomm
- Hvad er stammepolen?
- Paris e-scootere under pres for at bevise grønne legitimationsoplysninger
- Kan geotermiske energiprojekter forårsage jordskælv?
- Undersøgelse forstyrrer venturekapitalistiske antagelser om skattefordele for virksomheder
- Bioassisteret nanofotokatalysator til brintproduktion
- Sådan forklarer du fraktioner Trin for trin


