Har ilt det samme oxidationsnummer i ozon O3 og ilt O2?
* ilt (O2): I det diatomiske iltmolekyle deler de to iltatomer lige elektroner. Dette resulterer i et oxidationsnummer på 0 for hvert iltatom.
* ozon (O3): Ozon har en mere kompleks struktur. Det centrale iltatom danner enkeltbindinger med de to andre iltatomer. På grund af forskellen i elektronegativitet mellem iltatomer har det centrale iltatom en delvis negativ ladning, mens de to andre iltatomer har en delvis positiv ladning. Dette fører til et oxidationsnummer -1 For det centrale iltatom og +1 For de to andre iltatomer.
Derfor er oxidationsantallet af ilt i ozon (O3) ikke det samme som i ilt (O2).
Sidste artikelHvorfor katalysator reagerer ikke med reaktanterne?
Næste artikelEr NAC2H3O2 og HCH3O2 en buffer i vand?
 Varme artikler
Varme artikler
-
 Bøjelig beton og andre kulstof-infunderede cementblandinger kan dramatisk reducere de globale emiss…Bøjelig beton skabt ved University of Michigan giver mulighed for tyndere strukturer med mindre behov for stålarmering. Kredit:Joseph Xu/University of Michigan College of Engineering En af de stor
Bøjelig beton og andre kulstof-infunderede cementblandinger kan dramatisk reducere de globale emiss…Bøjelig beton skabt ved University of Michigan giver mulighed for tyndere strukturer med mindre behov for stålarmering. Kredit:Joseph Xu/University of Michigan College of Engineering En af de stor -
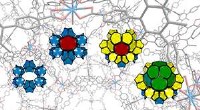 To simple byggeklodser producerer komplekst 3D-materialeSelvmontering af et metal-organisk stel. Kredit:Northwestern University Forskere fra Northwestern University har bygget et strukturelt komplekst materiale fra to simple byggesten, der er den metal
To simple byggeklodser producerer komplekst 3D-materialeSelvmontering af et metal-organisk stel. Kredit:Northwestern University Forskere fra Northwestern University har bygget et strukturelt komplekst materiale fra to simple byggesten, der er den metal -
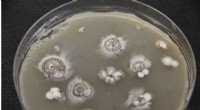 Forskere finder potentielle sygdomsbekæmpende sprænghoveder gemt i bakterierDyrkning af en thiocarboxylsyre producerende stamme af bakterier. Kredit:Shen Lab / The Scripps Research Institute Bakterier fundet i jord kan indeholde en potentiel game-changer for lægemiddeldes
Forskere finder potentielle sygdomsbekæmpende sprænghoveder gemt i bakterierDyrkning af en thiocarboxylsyre producerende stamme af bakterier. Kredit:Shen Lab / The Scripps Research Institute Bakterier fundet i jord kan indeholde en potentiel game-changer for lægemiddeldes -
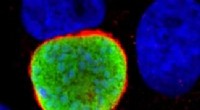 Malaria kaprer dine gener for at invadere din leverI de tidlige stadier af infektion, malariaparasitten (grøn) gemmer sig i en persons leverceller (blå), før den invaderer deres blod. Vist med rødt er et menneskeligt protein, som parasitten co-opterer
Malaria kaprer dine gener for at invadere din leverI de tidlige stadier af infektion, malariaparasitten (grøn) gemmer sig i en persons leverceller (blå), før den invaderer deres blod. Vist med rødt er et menneskeligt protein, som parasitten co-opterer
- Molekylær sondekort forkert foldet proteometilstand i levende celler
- Sådan fungerer Bradley-kampkøretøjer
- NASA gennemfører rumvandring, da verdens første rumvandrer dør
- 3D-struktur af kunstigt designet proteinnanopartikel TIP60 belyst ved kryo-elektronmikroskopi
- Hvad er de to nærmeste planeter, som nabo planeten Neptune?
- Udtalelse:Hvorfor vi underskrev det åbne brev fra videnskabsmænd, der støtter et totalt forbud mo…


