Temperaturen på en gas er?
Her er en sammenbrud:
* kinetisk energi: Dette er den energi, et objekt besidder på grund af dets bevægelse.
* molekyler: Gasser består af små partikler kaldet molekyler.
* gennemsnit: Temperaturen afspejler ikke den kinetiske energi i et enkelt molekyle, men den gennemsnitlige energi for alle molekyler i gassen.
Tænk på det på denne måde:
Forestil dig en flok små kugler, der hopper rundt i en beholder. Jo hurtigere kuglerne bevæger sig, jo højere er deres gennemsnitlige kinetiske energi og jo varmere gassen. Jo langsommere kugler bevæger sig, jo lavere er deres gennemsnitlige kinetiske energi og den koldere gassen.
Nøglepunkter:
* Temperatur er en grundlæggende egenskab for gasser.
* Højere temperatur betyder hurtigere molekylær bevægelse.
* Temperatur måles i enheder som Celsius (° C), Fahrenheit (° F) eller Kelvin (K).
 Varme artikler
Varme artikler
-
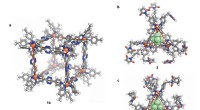 Kovalent post-montage modifikationskaskade af selvsamlede supramolekylære strukturerAfbildninger (samme skala) af røntgenkrystalstrukturerne. en, Terning 1b. b, PF6 − addukt af tetraeder 3. c, AsF6 - addukt af modificeret tetraeder 4a. Atomfarver:grå, C; hvid, H; rød, O; blå, N; oran
Kovalent post-montage modifikationskaskade af selvsamlede supramolekylære strukturerAfbildninger (samme skala) af røntgenkrystalstrukturerne. en, Terning 1b. b, PF6 − addukt af tetraeder 3. c, AsF6 - addukt af modificeret tetraeder 4a. Atomfarver:grå, C; hvid, H; rød, O; blå, N; oran -
 Flydende krystaller skaber letlæselige, farveskiftende sensorerPME-forskere og ingeniører har udviklet en måde at strække og spænde flydende krystaller på for at generere forskellige farver. Dette kunne anvendes i smarte belægninger, sensorer, og bærbar elektroni
Flydende krystaller skaber letlæselige, farveskiftende sensorerPME-forskere og ingeniører har udviklet en måde at strække og spænde flydende krystaller på for at generere forskellige farver. Dette kunne anvendes i smarte belægninger, sensorer, og bærbar elektroni -
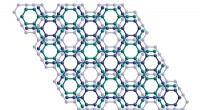 Langhypoteseret næste generations vidundermateriale skabt for første gangKrystalstrukturen af et lag af grafyn. Kredit:Yiming Hu I over et årti har forskere forsøgt at syntetisere en ny form for kulstof kaldet grafyn med begrænset succes. Den bestræbelse er dog nu ved
Langhypoteseret næste generations vidundermateriale skabt for første gangKrystalstrukturen af et lag af grafyn. Kredit:Yiming Hu I over et årti har forskere forsøgt at syntetisere en ny form for kulstof kaldet grafyn med begrænset succes. Den bestræbelse er dog nu ved -
 Nyt avanceret materiale viser ekstraordinær stabilitet over et bredt temperaturområdeForskere fra UNSW har fundet et ekstraordinært materiale, der ikke udvider sig eller trækker sig sammen over et ekstremt bredt temperaturområde og kan være et af de mest stabile materialer, man kender
Nyt avanceret materiale viser ekstraordinær stabilitet over et bredt temperaturområdeForskere fra UNSW har fundet et ekstraordinært materiale, der ikke udvider sig eller trækker sig sammen over et ekstremt bredt temperaturområde og kan være et af de mest stabile materialer, man kender
- Video:Verdens vanddag – hvad har rummet med det at gøre?
- Hvad er et præstationsfremmende lægemiddel? Her er 10 eksempler
- Et flygtigt øjeblik i tiden
- Hvor mange hundrededele er der i en kilometer?
- Noget energi fra solen reflekteres tilbage til hvad?
- Hvordan en kandidat ser ud kan svinge din stemme (uden at du selv er klar over det)


