Hvilken type binding dannes mellem atomer fast kobolt?
Her er hvorfor:
* Metallisk binding er en type kemisk binding, der forekommer mellem metalatomer.
* Ved metallisk binding delokaliseres valenselektronerne af metalatomerne, hvilket betyder, at de ikke er forbundet med noget særligt atom, men snarere bevæger sig frit gennem hele metallitteret.
* Denne delokalisering af elektroner resulterer i en stærk attraktion mellem de positivt ladede metalioner og det negativt ladede elektron "hav", der holder metalatomerne sammen i en stærk og stiv struktur.
Cobalt er et overgangsmetal, og ligesom andre overgangsmetaller udviser det metallisk binding. Dette er grunden til, at Cobalt er en god leder af elektricitet og varme, har et højt smeltepunkt og er formbar og duktil.
Sidste artikelHvad er den molekylære formel for methylbutan?
Næste artikelHvad er atommassen af ortophospharinsyre?
 Varme artikler
Varme artikler
-
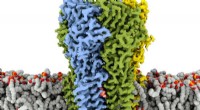 Undersøg detaljer om, hvordan generel bedøvelse og benzoer virker på receptorer i hjernenEn tredimensionel struktur af typen A GABA-receptor bundet med GABA og propofol indlejret i en cellemembran. Propofol er det mest almindeligt anvendte intravenøse bedøvelsesmiddel og virker gennem rec
Undersøg detaljer om, hvordan generel bedøvelse og benzoer virker på receptorer i hjernenEn tredimensionel struktur af typen A GABA-receptor bundet med GABA og propofol indlejret i en cellemembran. Propofol er det mest almindeligt anvendte intravenøse bedøvelsesmiddel og virker gennem rec -
 Yderligere to polymorfer fundet for rød-orange-gulKredit:ACS En trio af forskere ved Université de Montréal har opdaget yderligere to polymorfer for ROY, hvilket bringer det samlede antal til 10. I deres papir udgivet i Journal of the American C
Yderligere to polymorfer fundet for rød-orange-gulKredit:ACS En trio af forskere ved Université de Montréal har opdaget yderligere to polymorfer for ROY, hvilket bringer det samlede antal til 10. I deres papir udgivet i Journal of the American C -
 Biokemikere afslører indsigt i ekstraordinær regenerativ evneIana Kim, første forfatter til den nye undersøgelse, i et laboratorium for forskningsgruppen Gene Regulation by Non-coding RNA ved University of Bayreuth. Kredit:Christian Wißler Planarer er flado
Biokemikere afslører indsigt i ekstraordinær regenerativ evneIana Kim, første forfatter til den nye undersøgelse, i et laboratorium for forskningsgruppen Gene Regulation by Non-coding RNA ved University of Bayreuth. Kredit:Christian Wißler Planarer er flado -
 Opbygning af en bedre biosensorpolymerFlere kritiske udfordringer blev overvundet for at udvikle den nye type polymer, der har et stort potentiale for næste generations biosensorer. Kredit:KAUST; Xavier Pita Der er udviklet et nyt org
Opbygning af en bedre biosensorpolymerFlere kritiske udfordringer blev overvundet for at udvikle den nye type polymer, der har et stort potentiale for næste generations biosensorer. Kredit:KAUST; Xavier Pita Der er udviklet et nyt org
- Hvad er trykket 100 m under overfladen med densitet 1150 kgm3?
- hvad alle mineralerne?
- 7 iøjnefaldende fakta om Bright Star Vega
- Forskere skaber nye materialer, der kan øge stabiliteten af perovskit-solceller
- Ultrahurtige kvantesimuleringer:Et nyt twist til en gammel tilgang
- Forskere opdager en ny måde at målrette mod lægemiddelresistente bakterier på


